Vorwort
Ja, wir sind keine Radiologen. Ja, in der heutigen Zeit, in der es immer mehr um medikolegale Konsequenzen unseres Tuns geht, sollten wir uns nicht überschätzen und selbst radiologische Befunde erheben ohne die formale Qualifikation dafür zu haben. Ja, auch fachärztliche radiologische Befunde sind oft falsch (oder mindestens diskutabel). Ja, ich erwarte von allen Ärzten in Weiterbildung, dass sie sich die radiologischen Bilder unserer Patienten selbst anschauen.
Das MRT gilt dabei als besonders kompliziert. Das schöne ist aber – anders als Röntgenaufnahmen des Thorax – ist es das eigentlich gar nicht, und jede und jeder kann sich MRT-Aufnahmen orientierend anschauen.
Was technisches
Das müssen wir kurz halten. Ich versteh nämlich erschreckend wenig von der Technik hinter der MRT-Bildgebung (okay, sie ist auch ziemlich kompliziert und auch die meisten Radiologen können einem die technischen Hintergründe nicht wirklich erklären). Der Wikipedia-Artikel zur Kernspintomographie ist zumindest weitestgehend unverständlich (für einen mäßig begabten Mediziner), aber ein ganz klein wenig habe ich dann aber doch verstanden.
Die Grundidee der Kernspintomographie besteht darin, die Magnetisierbarkeit von Atomen zu nutzen, insbesondere von Wasserstoffatomen (Protonen). Durch das Anlegen verschiedener Magnetfelder geraten die Protonen in unterschiedliche Schwingungszustände, die genutzt werden können, um den Ort der Protonen zu bestimmen und Schnittbilder zu erzeugen.
Spin- und Gradienten-Echo-Sequenzen
Bei der MRT werden im Wesentlichen zwei Techniken angewendet: Spin-Echo- und Gradienten-Echo-Aufnahmen. Diese bilden die Grundlage für die verschiedenen MRT-Sequenzen, die wir kennen.
| Spin Echo | Gradienten Echo |
|---|---|
| T2 TSE | T1 |
| FLAIR | T1 mit Kontrastmittel |
| STIR | TOF |
| T2* |
| DWI |
Aus der Tabelle geht hervor, dass T1-Sequenzen im Wesentlichen Gradienten-Echo-Aufnahmen sind, T2-Wichtungen eigentlich immer Spin-Echo-Sequenzen (bis auf die T2*-Wichtung). Was ist nun aber der Unterschied?
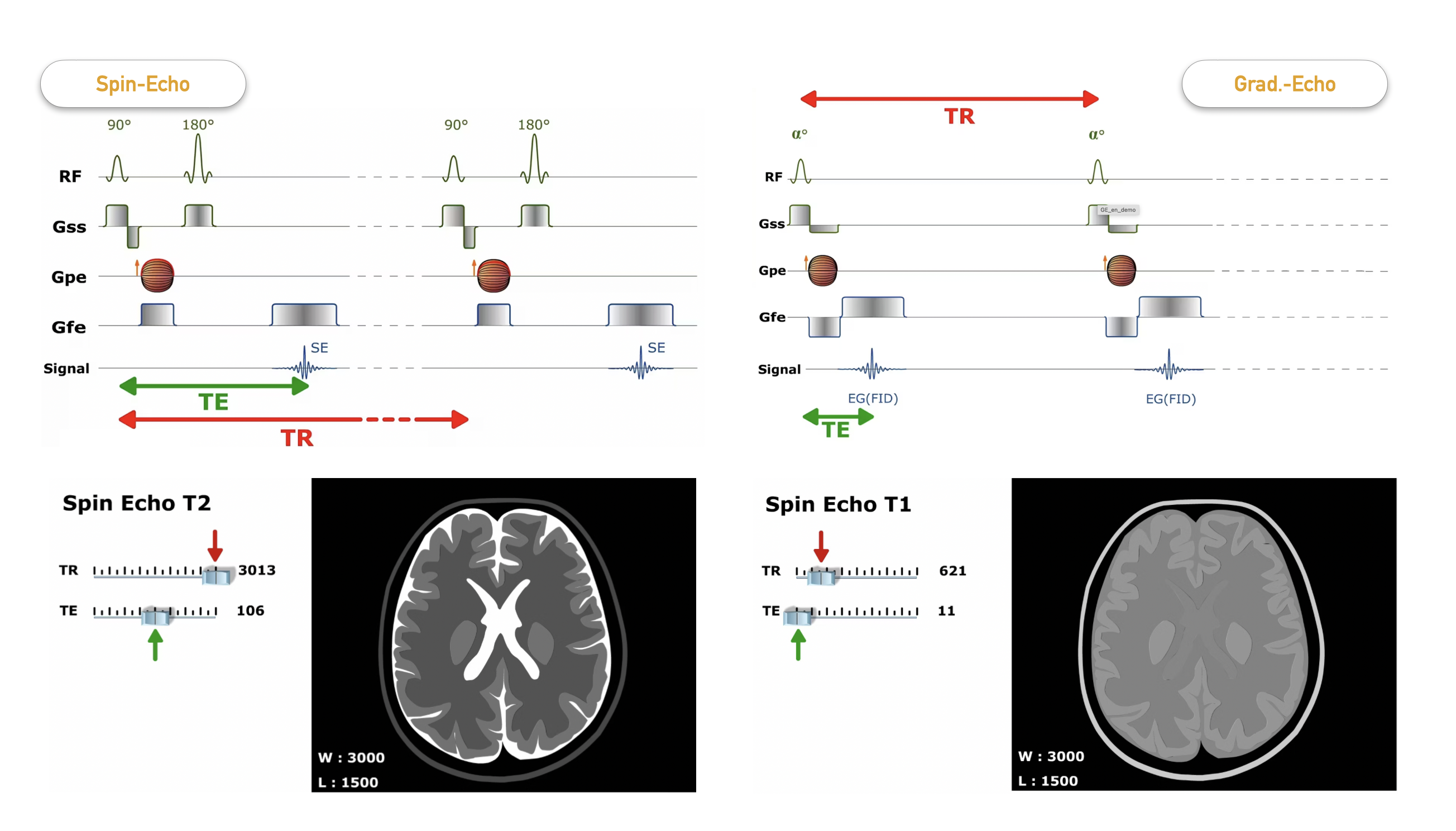
Beim Spin-Echo-Verfahren besteht der Schlüssel darin, dass zwei RF-Impulse mit verschiedenen Winkeln (90°/180°) gesendet werden, um die Protonen in einen Spin zu versetzen. Die Zeit zwischen dem ersten Impuls und dem Eintreffen des Signals ist einstellbar und wird als Echozeit (TE) bezeichnet. Auch die Zeit bis zur nächsten Sequenz, also bis zum nächsten 90°-Impuls, kann eingestellt werden. Dies ist die Relaxationszeit (TR). Beim Gradienten-Echo-Verfahren bleibt der Winkel des RF-Impulses konstant, und insgesamt sind TE und TR bei den T1-Sequenzen deutlich kürzer als bei den T2-Aufnahmen. Durch diese variablen (Zeit-)Einstellungen entstehen letztendlich die unterschiedlichen Kontraste und Bildcharakteristika.
Was Tempo-Taschentücher und MRT-Sequenzen gemeinsam haben
Die Bezeichnungen der Sequenzen, die wir täglich verwenden, variieren von MRT-Gerätehersteller zu MRT-Gerätehersteller leicht. Daher wird das, was die meisten von uns als FLAIR-Sequenz kennen, manchmal auch TIRM genannt, und die dünnschichtige T2-Sequenz, mit der der Kleinhirnbrückenwinkel gut dargestellt werden kann, trägt je nach Hersteller den Namen CISS, DRIVE oder FIESTA.
Mit 8 MRT-Sequenzen durchs Neurologen-Leben kommen
Um die allermeisten Bildgebungs-Fragestellungen beantworten zu können, reicht es, acht MRT-Sequenzen zu kennen und mit ihnen umgehen zu können.
T2-Wichtungen
Bei den T2-Sequenzen sind dies die T2 TSE, die FLAIR und die T2* (oder bei unserem Gerät T2 FFE).

T2 TSE (T2 Turbo Spin Echo) und FLAIR (Fluid-attenuated inversion recovery) (Link Doccheck) zeigen ähnliches Signalverhalten bei Gliosen und Gewebeödemen: Diese erscheinen hyperintens (also weiß). Ein Hauptunterschied besteht darin, dass in der T2 TSE auch der Liquor weiß erscheint, während er in der FLAIR „genullt“ wurde und somit schwarz erscheint. Dies erleichtert die Abgrenzung von Gewebeschäden und Liquorraum. Allerdings ist die Auflösung der T2 TSE deutlich besser. Die T2* ist – wie bereits erwähnt – eine Gradienten-Echo-Sequenz und dient zum Nachweis von Eisenablagerungen (also altem Blut). Frisches Blut hingegen zeigt sich besser in den T1-gewichteten Sequenzen.
T1-Wichtungen
Es gibt drei T1-Wichtungen, die es sich zu merken lohnt: Die T1 mit und ohne Kontrastmittel und die TOF-Angiographie.

Die T1 ohne Kontrastmittel wird hauptsächlich verwendet, um frisches Blut zu erkennen. Ansonsten dient sie als Substraktions-Sequenz für T1-Aufnahmen mit Kontrastmittel. Die T1 ist – wie häufig zu lesen ist – die einzige Sequenz, die die Anatomie des Gehirns korrekt wiedergibt: Die graue Substanz erscheint grau, die weiße Substanz weiß. Dies ist im klinischen Alltag jedoch nur bedingt relevant. Nach der Gabe von MRT-Kontrastmittel können in T1-Sequenzen gut frische entzündliche Läsionen und Raumforderungen abgegrenzt werden.
Mit der TOF (time of flight)-Angiographie können Protonen, die sich in einem bestimmten Geschwindigkeitsbereich in eine Richtung bewegen detektiert werden, so dass sich hieraus Kontrastmittel- und interventionsfreie Gefäßdarstellungen ableiten lassen.
Diffusionswichtungen
Zuletzt sind zwei Diffusionswichtungen von wesentlicher Bedeutung: Die B1000-Wichtung und die ADC-Map.

Es gibt eine Vielzahl von Diffusionswichtungen (Link Doccheck). Diese werden nach der Stärke der Signalabschwächung durch die Diffusion der Protonen durch das Gewebe benannt. B gibt dabei die Stärke der Signalabschwächung an. Für die meisten von uns ist die B1000 die geläufigste Sequenz. In den Diffusionswichtungen leuchtet das Signal dort weiß, wo eine Diffusionsstörung durch das Gewebe vorliegt, und erscheint schwarz, wo die Protonen ungehindert diffundieren können (z.B. im Liquor). Ein weißer Fleck in der Diffusionskarte bedeutet jedoch nicht zwangsläufig, dass es sich um einen akuten Hirninfarkt handelt, sondern lediglich, dass hier eine Diffusionsstörung vorliegt. Diffusionsstörungen können durch zytotoxische Ödeme (wie bei Infarkten, aber auch bei Entzündungen) und durch sehr zellreiche Läsionen entstehen (z.B. Lymphome oder Abszesse). Der klinische Kontext ist neben dem bildgebenden Muster also äußerst wichtig, um eine Diffusionsstörung richtig einzuschätzen.
Technisch gesehen sind Diffusionswichtungen eine Art Hybrid zwischen T1- und T2-Sequenzen. Starke T2-Signale (z.B. durch größere Narben oder Ödeme) können auch zu einer Signalanhebung in der Diffusionswichtung führen (T2-Durchscheineffekt), ohne dass eine tatsächliche Diffusionsstörung vorliegt. Hier kommt die ADC-Karte (Apparent Diffusion Coefficient) ins Spiel. Die ADC-Karte wird aus den Messwerten der Diffusionsmessungen berechnet und muss überall dort, wo eine „echte“ Diffusionsstörung vorliegt, abgesenkt und somit schwarz sein.
Usecases
Wie geht man nun praktisch vor? Ich habe mal die häufigsten Fragestellungen aufgeschrieben.
Hirninfarkt
Das, was uns alle am allermeisten interessiert ist, hat unser Patient/unsere Patientin „was frisches“. Also werden wir in der Regel in die B1000-Sequenz gucken (und idealerweise auch in die ADC-Karte).

Dann interessiert uns, ob es bereits ältere Hirninfarkte gibt und wie diese verteilt sind (und beim wake up-Schlaganfall, ob es ein Diffusions-FLAIR-Mismatch gibt). Die TOF-Angiographie bietet eine hochauflösende intrakranielle Angiographie. Stolperfallen hierbei sind Stellen mit Richtungswechseln (Carotis-Siphon) und höhergradige Stenosen. Durch die Einstellung eines Geschwindigkeitskorridors, in dem Protonenbewegungen gemessen werden, werden sehr schnelle und sehr langsame Flussgeschwindigkeiten nicht angezeigt, was zu falschen Schlussfolgerungen über Gefäßverschlüsse führen kann. Mit der T2*-Wichtung kann man schauen, ob es alte Blutungsresiduen gibt und natürlich, ob ein akuter Infarkt eingeblutet hat.

Entzündung / Tumor
Bei der Fragestellung Entzündung/Tumor benötigen wir im Wesentlichen drei Sequenzen: FLAIR, T1 mit und T1 ohne Kontrastmittel. Die FLAIR-Wichtung zeigt uns Ödeme und Gliosen, während T1-KM-Aufnahmen frische entzündliche Läsionen und Neoplasien gut darstellen können. Die Diffusionswichtung spielt – meiner Meinung nach zu Unrecht – eine Nischenrolle. Wie oben beschrieben, ist die Diffusionswichtung bei der Frage nach Abszessen und Lymphomen äußerst hilfreich.


Neurodegeneration
Bei der Abklärung neurodegenerativer Erkrankungen kommen wir hauptsächlich mit T2-Wichtungen aus. Während bei Schlaganfällen und Tumor/Entzündung die FLAIR aufgrund ihrer Liquorsättigung der T2 überlegen ist, verhält es sich hier umgekehrt. Bei neurodegenerativen Erkrankungen geht es hauptsächlich um die Detektion fokaler Atrophiemuster. Hier ist es oft einfacher, derartige Muster mithilfe der hochauflösenden T2 und dem starken Kontrast zwischen grauem Hirngewebe und weißem Liquor zu erkennen.

Besonders wichtig ist es, bei neurodegenerativen Erkrankungen eine sagittale T2-gewichtete Sequenz zu haben. Zum einen, um bei atypischen Parkinson-Syndromen Mittelhirnatrophien besser abgrenzen zu können, und zum anderen, um bei der Frage nach einem Normaldruckhydrocephalus einen flow void über dem vierten Ventrikel darstellen zu können.
Spinale Bildgebung
Bei der Betrachtung der Bildgebung von Wirbelsäule und Rückenmark gibt es eine Grundregel: Bildbetrachter immer in zwei Spalten teilen, auf der einen Seite die sagittale T2 laden, auf der anderen Seite die axialen Bilder. Es ist viel einfacher, sich anhand der sagittalen Darstellung zu orientieren (da man Wirbelkörper zählen kann), als dies mit den axialen Bildern zu versuchen. Wenn dann sagittal eine Auffälligkeit gefunden wurde, kann diese Höhe in den axialen Schnitten eingestellt werden, um bei z.B. Bandscheibenvorfällen oder Myelitiden eine eventuelle Seitenbetonung zu erkennen. Genauso geht man bei den KM-Sequenzen vor.
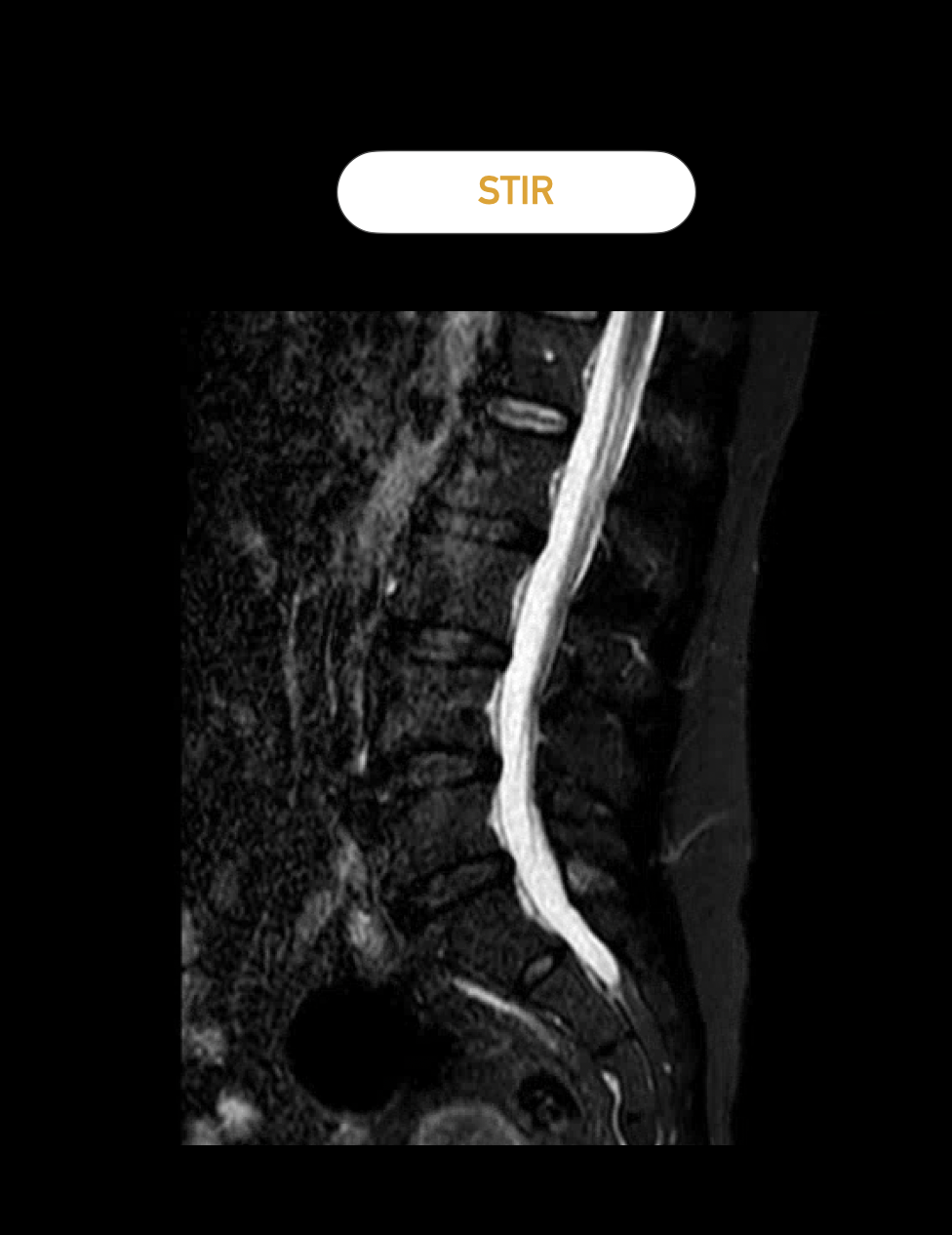
Die STIR-Sequenz ist ebenfalls eine T2-Wichtung, zeigt aber besonders gut Knochenödeme. Bei der Frage nach Wirbelkörperfrakturen ist dies besonders hilfreich.

Fazit
Auch Nicht-Radiologen wie Neurologen (und solche in Weiterbildung) sollten sich regelmäßig die Schnittbildgebung ihrer Patienten anschauen, auch wenn sie formell keine abschließenden Befunde erstellen dürfen. Die MRT-Bildgebung ist viel unkomplizierter, als man zunächst denken mag. Um einen guten Überblick zu erhalten, genügt es, einigermaßen sicher mit gerade mal acht Sequenzen umgehen zu können.
Titelbild by KasugaHuang, CC BY-SA 3.0
Hinterlasse einen Kommentar