Im Zuge meiner Schmerzmedizin-Prüfung hatte ich zu Beginn des Blogs im August 2020 einen Beitrag zum komplexen regionalen Schmerzsyndrom (CRPS) geschrieben (Link). Knapp fünf Jahre sind aber eine lange Zeit, so dass ich den Text angesichts eines Vortrags zum CRPS, welchen ich halten durfte, noch einmal überarbeitet habe.
CRPS: Was ist das eigentlich ?
Versucht man sich an einer Definition zum CRPS, so landet man unweigerlich bei einer, welche folgende Punkte beinhaltet:
Das CRPS ist eine chronische Schmerzstörung, welche durch starke, anhaltende Schmerzen gekennzeichnet, die in keinem Verhältnis zum ursprünglichen Auslöser (meist einer Extremitätenverletzung wie einer Fraktur) stehen. Typische weitere Symptome sind:
- Sensibilitätsstörungen: Hier finden sich im wesentlichen Charakteristika einer neuropathischen Schmerzstörung, nämlich eine Überempfindlichkeit gegenüber Schmerzreizen (Hyperalgesie) und Schmerzen, welche durch eigentlich nicht schmerzhafte Reize ausgelöst werden (mechanische Allodynie).
- Motorische Einschränkungen: Typische Symptome sind Bewegungseinschränkungen, Muskelatrophie und Tremor-Syndrome. Zudem ist häufig ein Pseudoneglekt zu beobachten, eine Vernachlässigung des betroffenen Körperteils, ohne dass ein Neglekt im klassischen neuropsychologischen Sinne besteht).
- Vegetative und sudomotorische Störungen: Am häufigsten treten Schwellungen, Farb- oder Temperaturveränderungen der Haut, abnormales Schwitzen und Veränderungen von Haar- oder Nagelwachstum auf.
Blickdiagnose CRPS?
Gerade das Vollbild eines CRPS ist eigentlich eine Blickdiagnose. Relevante Differentialdiagnosen existieren bei einem komplett ausgeprägten CRPS kaum, bzw. erscheinen sehr bemüht.


Epidemiologie: Wer ist betroffen?
Das CRPS gilt als seltene Erkrankung, aber wie es mit seltenen Erkrankungen so ist, sind sie in der Gesamtheit dann gar nicht mehr so selten. Die Inzidenz des CRPS beträgt 5–6 pro 100.000 Personen, die Häufigkeit, mit der es nach Extremitätenverletzungen auftritt, wird in verschiedenen Studien zwischen 1 und 37% quantifiziert. Besonders tritt das CRPS auf:
- nach distalen Radiusfrakturen (bis zu 37 %), damit deutlich häufiger als nach peripheren Nervenverletzungen (bis zu 5 %).
- überwiegend an den oberen Extremitäten (zwei Drittel der Fälle), weniger an den unteren Extremitäten (ein Drittel der Fälle).
- häufiger bei Frauen als bei Männern (Verhältnis 2–3 : 1) und im mittleren Lebensalter zwischen 40 und 70 Jahren.
- wenn bestimmte Risikofaktoren vorliegen (depressive Störungen, Rauchen und hohe Schmerzintensität kurz nach dem Trauma).
Diagnose: Die Budapest-Kriterien
Die Budapest-Kriterien, eingeführt im Jahr 2010, operationalisieren das CRPS neu und erreichen eine hohe Sensitivität von 99 % und eine Spezifität von 78 %. Diese Kriterien lösten die vorherigen IASP-Kriterien ab, die sich als zu unspezifisch erwiesen hatten (vgl. Harden et al.). Die Budapest-Kriterien folgen dem üblichen Format für die Diagnose von Schmerzsyndromen, indem sie eine Reihe von Symptomen definieren, von denen eine bestimmte Anzahl erfüllt sein muss, und schließen mit der üblichen Ausschlussklausel: „Eine andere Erkrankung erklärt die Symptomatik nicht hinreichend.“
Budapest-Kriterien des CRPS
1) Anhaltender Schmerz, der durch das Anfangstrauma nicht mehr erklärt wird
2) Die Patienten müssen über jeweils mindestens 1 Symptom aus 3 der 4 folgenden Kategorien in der Anamnese berichten:
a. Hyperalgesie (Überempfindlichkeit für Schmerzreize); „Hyperästhesie“ (Überempfindlichkeit für Berührung, Allodynie)
b. Asymmetrie der Hauttemperatur; Veränderung der Hautfarbe
c. Asymmetrie des lokalen Schwitzens; Ödem
d. Reduzierte Beweglichkeit, Dystonie, Tremor, „Paresen“ (im Sinne von Schwäche); Veränderungen von Haar- oder Nagelwachstum
3) Bei den Patienten müssen jeweils mindestens 1 Symptom aus 2 der 4 folgenden Kategorien zum Zeitpunkt der Untersuchung vorliegen:
a. Hyperalgesie auf spitze Reize (z.B. Zahnstocher); Allodynie; Schmerz bei Druck auf Gelenke/Knochen/Muskeln
b. Asymmetrie der Hauttemperatur; Veränderung der Hautfarbe
c. Asymmetrie des lokalen Schwitzens; Ödem
d. Reduzierte Beweglichkeit, Dystonie, Tremor, „Paresen“ (im Sinne von Schwäche); Veränderungen von Haar- oder Nagelwachstum
4) Eine andere Erkrankung erklärt die Symptomatik nicht hinreichend.
Die Tücken der Diagnose einer primär chronischen Schmerzstörung
Beim Versuch, das CRPS möglichst spezifisch zu operationalisieren, stößt man in der klinischen Praxis schnell auf eine Diskrepanz, die aus ärztlicher Sicht zutiefst unlogisch und sogar falsch erscheint. Im ICD-11, der insbesondere in der Psychiatrie (und damit auch in der Schmerzmedizin) bereits verwendet wird, wird das CRPS als primär chronische Schmerzstörung klassifiziert. Daher müssen die Symptome mindestens drei Monate andauern, bevor die Diagnose formal gestellt werden kann. Allerdings hat das CRPS eine deutlich bessere Prognose bei früher Behandlung. Daher werden in der klinischen Realität Fälle, bei denen ein CRPS vermutet wird, natürlich auch schon vor Ablauf der drei Monate behandelt. In diesen Fällen muss die Diagnose jedoch eigentlich noch als „Verdacht auf CRPS“ bezeichnet werden.
Apparative Zusatzdiagnostik
Bei eindeutigem Befund ist bei CRPS eigentlich keine weitere Zusatzdiagnostik erforderlich. Gerade in der Frühphase, in der die Diagnose formal noch nicht gestellt werden kann, bietet sich jedoch die 3-Phasen-Skelett-Szintigraphie an. Diese zeigt typischerweise eine bandförmige Mehranreicherung in den Gelenken der betroffenen Extremität. Die diagnostische Sicherheit wird durch die Szintigraphie deutlich erhöht, die in den ersten Monaten beim CRPS eine Sensitivität von 97% und eine Spezifität von 86% aufweist.

Ganz anders ist es beim konventionellen Röntgen der Extremitäten und der Frage nach Kalksalzminderungen gelagert. Diese Untersuchung spukt noch durch viele – lange auch durch meinen – Ärzte-Köpfe. Hier wird allerdings nur eine Sensitivität von 73% und eine Spezifität von 57% erreicht, ein guter Grund dieses Verfahren ersatzlos aus dem Repertoire bei der CRPS-Diagnostik zu streichen.
Typen- und Stadieneinteilung des CRPS: Dinge, die man getrost vergessen kann
Egal wie wenig Ahnung man vom Thema CRPS hat, eine Sache wissen alle: Das CRPS wird in zwei Typen unterteilt:
- Typ I (Morbus Sudeck): Ohne nachweisbare Nervenverletzung.
- Typ II (Kausalgie): Mit nachgewiesener Nervenverletzung.
Nur, das ganze hat für die Symptomatik, Diagnostik und Therapie des CRPS keinerlei Konsequenz. Beide Typen führen zu den selben Symptomen, werden gleich diagnostiziert und behandelt. Wenn eine strukturelle Nervenverletzung vorliegt, dann wird diese – hoffentlich – umgehend nach dem Trauma chirurgisch behandelt. Und wenn eine Nervenverletzung vorgelegen hat, kann es genauso gut auch zu keinem CRPS kommen, aber eben auch umgekehrt (was den viel häufigeren Fall darstellt).
Daher wird mittlerweile in vielen Arbeiten zum CRPS die Typ I/Typ II-Einteilung als obsolet betrachtet. Das selbe gilt für die Einteilung in die drei klassischen CRPS-Stadien:
- Akut (0–3 Monate): Entzündliche Schwellung, lokale Schmerzen, Sensibilitäts- und Bewegungsstörungen.
- Dystroph (3–6 Monate): Schmerzen werden diffuser, Gelenksteife, anhaltendes Ödem, Knochenentkalkung.
- Atrophisch (6–12 Monate): Schmerzen können nachlassen, aber es kommt zu irreversiblen Gewebeveränderungen und Funktionseinbußen.
Auch hier muss man feststellen, dass diese Stadien-Einteilung als überholt gelten muss. Symptome aus allen Stadien können zu allen Zeitpunkten auftreten.
Eine Einteilung, die eine gewisse Konsequenz hat, ist die in ein kaltes und ein warmes CRPS, was sich auf die initiale Hauttemperatur an der betroffenen Extremität bezieht. Dabei weiß man, dass ein initial warmes CRPS eine bessere Prognose als ein kaltes CRPS hat.
Wie entsteht so was: Pathogenese des CRPS
Nachdem lange Zeit wenig Bewegung im Verständnis der CRPS auf pathophysiologischer Ebene zu beobachten war, sind In den letzten fünf bis zehn Jahren sind einige Arbeiten erschienen, die hier deutlich mehr Licht ins Dunkel bringen konnten. Grob gesagt können offenbar vier zeitlich versetzt auftretende pathophysiologische Prozesse identifiziert werden: Den Gewebeschaden, welcher mit einer inflammatorischen Reaktion einhergeht, eine Störung der Schmerzverarbeitung, autonome und endokrine Reaktionen und eine immunologische Antwort.

Ein wesentlicher Teil der Entstehung des CRPS scheint der lokale Gewebeschaden zu sein, bei dem dendritische Zellen und DAMP (Damage-Associated Molecular Patterns) eine entscheidende Rolle spielen. DAMP sind im wesentlichen intrazelluläre Fragmente von zerstörten Zellen, also DNA-Fragmente, intrazelluläre Proteine usw. Diese werden vom Lymphsystem aufgenommen und führen dann in den Lymphknoten zu einer Aktivierung proinflammatorischer Zytokine, wie TNF-alpha, Interleukin-1 und Interleukin-6. Auf der anderen Seite kommt es relativ rasch im Bereich der Spinalganglien zu einer Mikroglia-Aktivierung, welche am Ende in einem neuronalen Schaden resultiert.
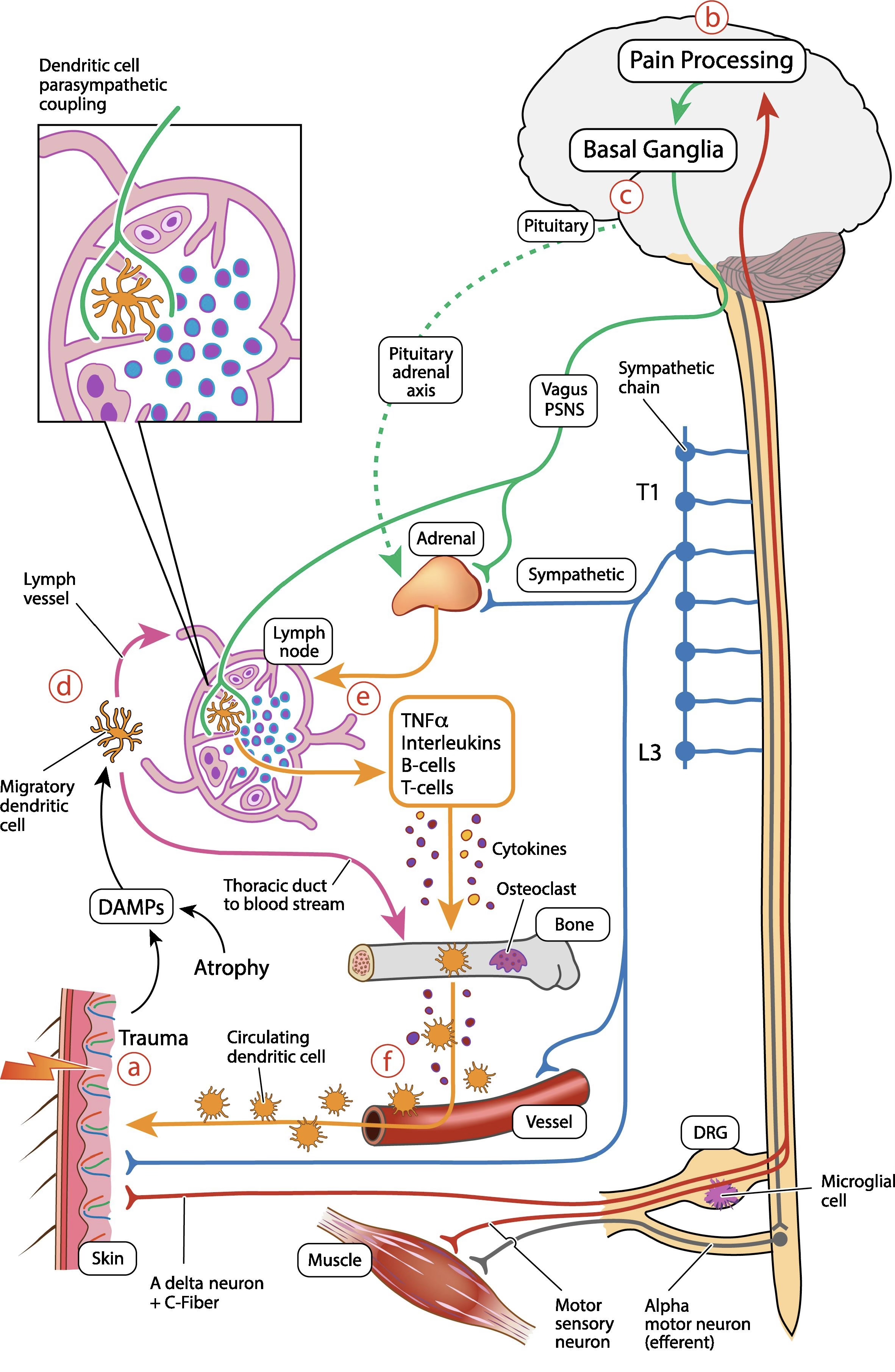
Von diesen beiden Ausgangspunkten scheint sich dann die mehrstufige Pathogenese-Kaskade zu entwickeln.
Therapie: Multimodaler Ansatz
Bei der Behandlung des CRPS hat sich in den letzten 10 Jahren tatsächlich ein Paradigmenwechsel zugetragen. Jahrelang war das Credo: „Ruhigstellen“. Noch in meinem Schmerzmedizin-Buch von 2017 (Maier, Diener, Bingel) findet sich zum CRPS folgende Feststellung:
Stufe A: Behandlung des Ruheschmerzes und des Ödems.
Solange diese beiden Symptome vorliegen, sind sie vorrangig zu behandeln, alle anderen Maßnahmen sind zunächst zweitrangig. Schonung und Immobilisation prägen diese erste Therapiephase. Alle Maßnahmen verfolgen das Ziel, den Patienten zunächst körperlich wie psychisch zu stabilisieren. Interventionen, die zu einer Schmerzverstärkung führen (Ergotherapie, ipsilaterale Krankengymnastik, psychischer Stress) sind in dieser Therapiephase kontraindiziert.
In den Papern zum CRPS wurde da schon längst „hands on“ als Therapieregime propagiert. Gleich geblieben ist aber die Grundauffassung, keine Schmerzverstärkung herbeizuführen. Somit ist schlussendlich alles erlaubt, was die Schmerzen nicht verstärkt und was eine aktive Mitarbeit des Patienten voraussetzt. Daher kann es hier sehr sinnvoll sein auch großzügig Analgetika einzusetzen, damit diese Therapieverfahren auch gut und rasch durchgeführt werden können.
Nicht-medikamentöse Therapie
Die nicht-medikamentöse Therapie steht bei der Behandlung des CRPS ganz im Fokus. Gute Evidenz gibt es für das Graded Exposure Training, bei dem die Trainingsintensität dem jeweiligen Schmerzempfinden angepasst wird und für die Spiegeltherapie. Umstrittener ist die „Pain Exposure Physical Therapy“, worunter man versteht, dass man mit der Zustimmung des Patienten physiotherapeutischen Übungen durchführt, die auch durchaus Schmerzen indizieren dürfen.
Medikamentöse Therapie
Die Studienlage zur medikamentösen Therapie beim CRPS ist relativ bescheiden. Gute Evidenz gibt es für die Behandlung des CRPS in der Frühphase mit Steroiden (30-40 mg Prednisolon für 2-12 Wochen) und mit Bisphosphonaten (eigentlich als i.v.-Gabe).
Da es sich bei den CRPS-Schmerzen um neuropathische Schmerzen handelt, ist die Behandlung wie bei anderen neuropathischen Schmerzsyndromen mit SSNRI, Trizyklika und Gabapentin oder Pregabalin sicher aus pathophysiologischen Erwägungen sinnvoll, eine explizite Testung gibt es aber nur für Gabapentin und tatsächlich für Ketamin i.v. als NMDA-Rezeptor-Antagonist (und für Memantine p.o. mit der selben Intention in Verbindung mit Morphin). All das hat aber nur „poor quality evidence“, dennoch wird man diese Medikamente, genau wie Opioide (ebenfalls nur „poor quality evidence“) aber regelhaft einsetzen und einsetzen müssen.
Dann wird es verrückt, es gibt eine Substanz namens Dimethylsulfoxid (DMSO), welche man topisch auftragen kann und welche normalerweise als Trägersubstanz dient, wenn man irgendwelche Stoffe über die Haut applizieren will (wenn ich das richtig verstanden habe z.B. Polonium, wenn man russischer Geheimdienst-Meuchel-Mörder ist). DMSO ohne Zusatz hat aber in einer Studie aus Holland gute Erfolge beim CRPS gezeigt.
Interventionelle Therapie
Ebenfalls mit schlechter Evidenz, aber häufig auf Grund von positiven Expertenmeinungen in den Behandlungszentren werden unter der Vorstellung eines „sympathisch unterhaltenen Schmerzes“ Sympathikusblockaden durchgeführt. Zunehmend mehr positive Berichte gibt es zudem für den Einsatz von Rückenmarksstimulatoren (SCS).
Prognose des CRPS
Mit einem CRPS hat man immer lange zu tun, dennoch gilt heutzutage, dass die Prognose bei weitem nicht mehr so desolat ist, wie vor wenigen Jahren, auch und gerade durch den früheren Therapiebeginn. Nach aktuellen Studien kann man mit einer frühen Therapie in bis zu 80% der Fälle eine Remission innerhalb von 12 Monaten erzielen.
Wo man weiterlesen kann
S1-Leitlinie Diagnostik und Therapie komplexer regionaler Schmerzsyndrome (CRPS) https://dgn.org/leitlinie/diagnostik-und-therapie-komplexer-regionaler-schmerzsyndrome-crps
Birklein, F., Ajit, S. K., Goebel, A., Perez, R. S. G. M. & Sommer, C. Complex regional pain syndrome — phenotypic characteristics and potential biomarkers. Nat. Rev. Neurol. 14, 272–284 (2018).
Lloyd ECO, Dempsey B, Romero L. Complex Regional Pain Syndrome. COMPLEX REGIONAL PAIN SYNDROME. 2021;104(1)..
Steenken L, Birklein F. Das komplexe regionale Schmerzsyndrom (CRPS). MMW – Fortschritte der Medizin. 2023
Weitere Literatur
Birklein, F. & Schlereth, T. Aktuelles zur Therapie des komplex-regionalen Schmerzsyndroms. Nervenarzt 84, 1436–1444 (2013).
Castillo-Guzmán S, Nava-Obregón TA, Palacios-Ríos D, et al. Complex regional pain syndrome (CRPS), a review. Medicina Universitaria. 2015;17(67):114-121.
David Clark, J., Tawfik, V. L., Tajerian, M. & Kingery, W. S. Autoinflammatory and autoimmune contributions to complex regional pain syndrome. Mol. Pain 14, 174480691879912 (2018).
Frettlöh, J., Hüppe, M. & Maier, C. Severity and specificity of neglect-like symptoms in patients with complex regional pain syndrome (CRPS) compared to chronic limb pain of other origins. Pain 124, 184–189 (2006).
Harden NR, Bruehl S, Perez RSGM, et al. Validation of proposed diagnostic criteria (the “Budapest Criteria”) for Complex Regional Pain Syndrome. Pain. 2010;150(2):268-274. doi:10.1016/j.pain.2010.04.030
Maier, Christoph, Diener, Hans-Christoph, Ringel, Ulrike(Hrsg.): Schmerzmedizin – Interdisziplinäre Diagnose- und Behandlungsstrategien, 5. Auflage, 2017
Maihöfner, C., Handwerker, H. O., Neundörfer, B. & Birklein, F. Cortical reorganization during recovery from complex regional pain syndrome. Neurology 63, 693–701 (2004).
Krumova, E., Maier, C. & Tegenthoff, M. Neues aus der Forschung zum Komplexen Regionalen Schmerzsyndrom (CRPS). Aktuelle Neurol. 40, 478–485 (2013).
Russo M, Georgius P, Santarelli DM. A new hypothesis for the pathophysiology of complex regional pain syndrome. Medical Hypotheses. 2018;119:41-53
Wolter, T., Knöller, S. & Rommel, O. Komplexes regionales Schmerzsyndrom bei Nervenwurzelkompression und nach Wirbelsäulenoperation. Der Schmerz 30, 227–232 (2016).
Hinterlasse einen Kommentar