Angetriggert von der Diskussion um p-tau217 als neuer Blut-Biomarker der Alzheimer-Krankheit,
meinem schlechten Gewissen und den guten Vorsätzen für den Blog dieses Jahr allen Widrigkeiten zum Trotz kommt hier eine kleine Reihe zur Alzheimer-Krankheit. Grundlage für alles weitere ist dieser – gar nicht so schlecht gealterte – Blogbeitrag von 2021:
Neurodegenerative Krankheiten: WYSIWYG oder nicht? Die Sache mit den Tauopathien und den Synukleinopathien.
Windows 95 und neurodegenerative Erkrankungen Den WYSIWYG-Vergleich wollte ich schon ganz lange machen. Heute soll es um neurodegenerative Erkrankungen gehen und um die Frage, ob es auch wirklich Parkinson ist, wenn es wie Parkinson ausschaut. WYSIWYG ist ja so ein Begriff der ungefähr aus der Ära von Karl Klammer und Windows 95 kommt. Ganz kurz…
In dem Artikel geht es um die verschiedenen neuropathogenen Proteine aus deren Veränderungen und Ausbreitungsmechanismus auf Zellebene neurodegenerative Erkrankungen resultieren. Heute soll es dann um die Frühdiagnostik gehen, im nächsten Beitrag um die ersten spezifischen Antikörper-Therapien und dann um Präventionsmöglichkeiten der Alzheimer-Krankheit.
Warum überhaupt Biomarker-Diagnostik? Kann man Alzheimer nicht klinisch diagnostizieren?
Doch, natürlich. Es gibt gute klinische Diagnosekriterien der Alzheimer-Krankheit. Diese beinhalten die charakteristische Alzheimer-Symptomatik:
- Schleichender (nicht akuter) Beginn und progredienter Verlauf über mindestens 6 Monate
- Es steht eine Gedächtnisstörung (v. a. Kurzzeitgedächtnisstörung) im Vordergrund.
- Es ist mindestens eine weitere kognitive Domäne beeinträchtigt:
- Sprache (Aphasie),
- exekutive Funktionen,
- visuell-räumliche Fähigkeiten,
- Aufmerksamkeit.
Zudem wird ein Ausschluss anderer Ursachen für die Symptomatik gefordert:
- Keine Hinweise auf andere primäre Demenzformen (z. B. vaskuläre Demenz, Lewy-Body-Demenz).
- Keine Hinweise auf delirante, psychiatrische oder internistische Ursachen (z. B. Depression, Hypothyreose, Vitamin-B12-Mangel).
- Kein Nachweis akuter struktureller Läsionen im CT oder Ausschluss über Anamnese/Befund
Demnach kann man die Diagnose sogar ohne MRT und mit einer relativ rudimentären Labordiagnostik stellen (das kommt dem Krankenhaus-Neurologen in mir immer noch komisch vor).
Typischerweise wird man die neuropsychologischen Auffälligkeiten mit mindestens einem Kurztest wie dem MoCA (Montreal Cognitive Assessment) oder – wenn möglich – einem CERAD objektivieren.
| MMST | Uhrentest nach Shulman | DemTect | MoCA | |
|---|---|---|---|---|
| Dauer | 10–12 Min | 2–5 Min | 8–10 Min | 10–20 Min |
| Kurzzeit-/Arbeitsgedächtnis (exekutive Funktionen) | + | + | ++ | +++ |
| Langzeitgedächtnis (Encodierung, hippocampusabhängig) | ++ | – | ++ | +++ |
| Sprachkompetenz | + | + | ++ | +++ |
| Abstraktionsvermögen | – | – | – | +++ |
| Aufmerksamkeit | + | – | ++ | +++ |
| Orientierung | ++ | – | – | +++ |
| Visuokonstruktion | + | ++ | – | +++ |
| Exekutivfunktionen | – | + | + | +++ |
| Apraxie | – | – | – | – |
| Anwendung | Schneller, weit verbreiteter Screeningtest; verbreitet zur Beurteilung des Schweregrades einer neurokognitiven Störung (leicht: 20–26; 10–19: mittelschwer; <10: schwer) | Gute Ergänzung zum DemTect zur Beurteilung der Visuokonstruktion; Beurteilung 1–6 Punkte | Basisdiagnostik Frühererkennung MCI u. Neurokognitiver Störungen; sensitiver und spezifischer für MCI und Neurokognitive Störungen als MMST; unterscheidet zwischen Kurzzeit- und Arbeitsgedächtnis (Zahlenreihen); Testwerte enthalten unterschiedliche Bewertung nach Alter, daher gilt Skala für alle Altersgruppen; Bereiche: 13–18: Keine Beeinträchtigung erkennbar; 9–12: Leichte kognitive Störung; 0–8: V.a. Neurokognitive Störung | Basisdiagnostik Frühererkennung MCI u. Neurokognitiver Störungen, auch bei Parkinson-Krankheit; bester Screeningtest; für MCI sensitiver als MMST; Bereiche: 26–30: Unauffällig, keine Einschränkungen; 6–25: Mindestens MCI; 0–5: extreme geistige Beeinträchtigung; für blinde oder sehbeeinträchtigte Menschen rein auditive Tests verfügbar; für gehörlose Menschen rein visuelle Versionen |
| Limitierungen | Keine Unterscheidung verschiedener Neurokognitiver Störungsformen (Alzh., vask. D., FTD); path. Ergebnisse sorgfältig zur Depression abgrenzen; extreme Anfälligkeit für Störeinflüsse; Leistung ist bildungs- und sprachabhängig und unterliegt Tagesschwankungen (Limitierung zur Einschätzung des Schweregrades); eingeschränkte Sensitivität für beginnende Neurokognitive Störungen | Nicht geeignet zur Untersuchung hippocampusabhängiger Gedächtnisleistungen; nur grobe, wenig differenzierte Beurteilung möglich; Leistungseinschränkungen können auf unterschiedliche Grundstörungen zurückgeführt werden (z.B. räumliche Defizite aber auch Einschränkungen im Bereich des Gedächtnisses, der exekutiven Leistungsfähigkeit oder der Sprache) | Testergebnisse können nicht in allen Altersstufen problemlos miteinander verglichen werden; bei Patienten <40 Jahre eignet sich der DemTect nicht als Screening; keine Einordnung des Schweregrad, daher für Verlaufskontrolle weniger geeignet als andere Tests; kein Anteil „Visuokonstruktion“ | Falsch positive Ergebnisse häufig (eingeschränkte Spezifität) |
| Anmerkungen | Verschiedene Versionen, aber keine Parallelformen | Verfahren suggeriert, dass eine valide Aussage möglich sei (über die Zuordnung der Testwerte); es liegen aber keine Normwerte vor; hoher Anteil an verbalen Aufgaben | In Anlehnung an CERAD erfolgt (CERAD = standardisierte Testung); dabei wurden die Itemdichte und damit die Genauigkeit verringert; Nähe zur CERAD limitiert aufgrund Lerneffekten eine spätere NP Testung |
Der Mini-Mental-Status-Test (MMST) ist für die Frühdiagnostik und zur Differenzierung der verschiedenen neuropsychologischen Störungsbilder eigentlich nicht trennscharf genug, hat aber weiter seinen Stellenwert, da über ihn die Schweregrade der Alzheimer-Krankheit unterschieden werden:
- Leichte kognitive Störung: MMST 25-27 Punkte
- Leichte Demenz: MMST 21–24 Punkte
- Mittelschwere Demenz: MMST 10–20 Punkte
- Schwere Demenz: MMST < 10 Punkte
Zusammenfassend – mit dem Wissen um die neuropathologischen Veränderungen – entsteht aus dem Gesagten dann in etwa folgendes Schema:
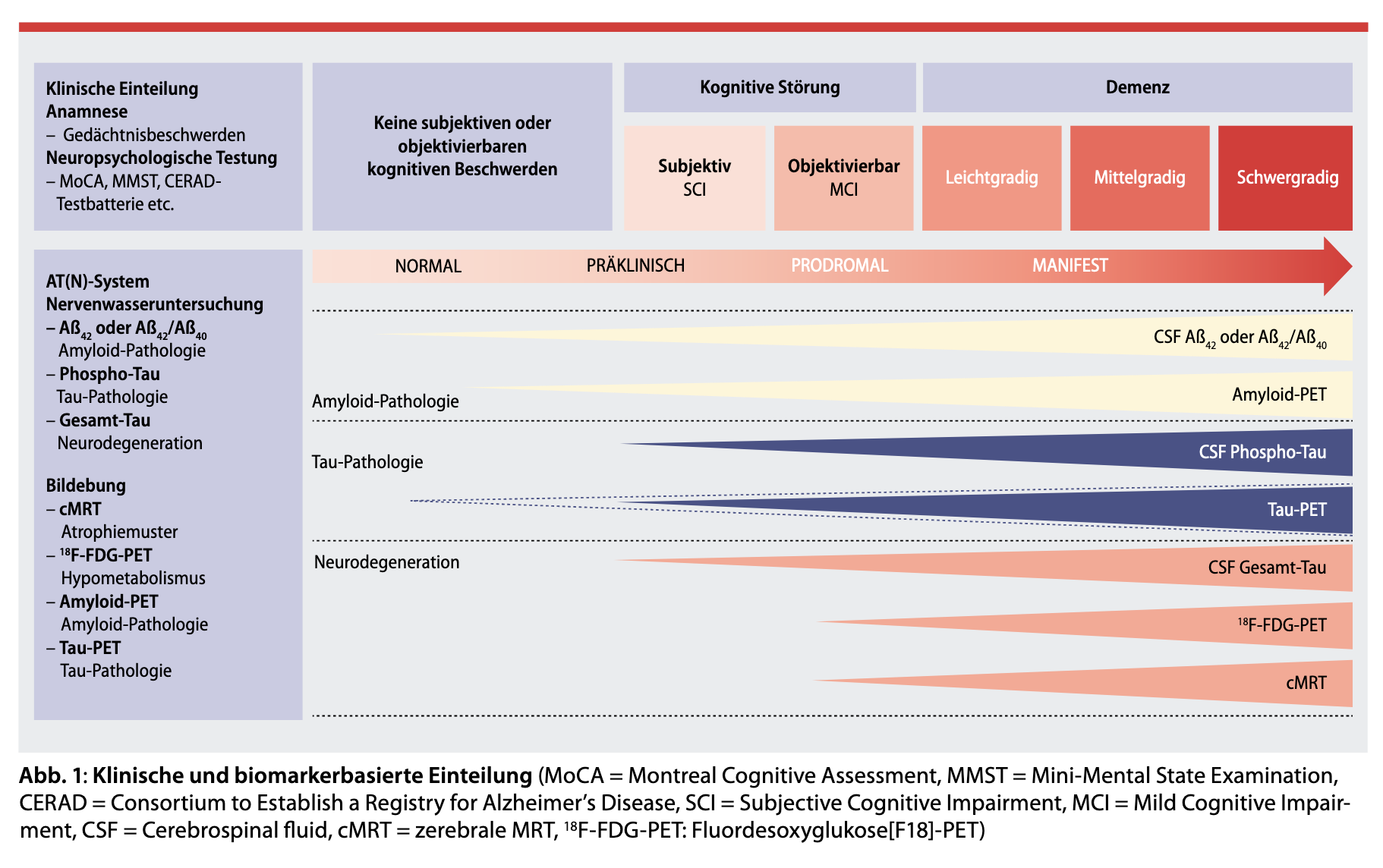
Wofür braucht es dann biomarkergestützte Diagnosekriterien?
Bei allen neurodegenerativen Erkrankungen manifestiert sich die Symptomatik – auch in den leichten Krankheitsstadien – erst, wenn auf zellulärer Ebene schon ein beträchtlicher Schaden eingetreten ist; bei der Alzheimer-Krankheit also viele Millionen Neuronen destruiert sind, es zu ß-Amyloid-Ablagerungen und einer deutlichen Tau-Proteinerhöhung gekommen ist. Möchte man diese neuropathologischen Vorgänge mit krankheitsmodifizierenden Therapieverfahren beeinflussen, so muss man möglichst frühzeitig im Krankheitsprozess behandeln, mindestens in leichten Krankheitsstadien, besser eigentlich noch bevor die Krankheit klinisch überhaupt ausbricht. Dies funktioniert aber nur, wenn man abseits der klinischen Diagnosekriterien (die dann ja noch nicht positiv sein dürften) weitere Befunde zur Hand hat, die den Krankheitsprozess eindeutig belegen. Und hier kommen die Biomarker ins Spiel.
Wie funktioniert Biomarker-Diagnostik bei der Alzheimer-Krankheit aktuell?
Das 2016 erstmals eingeführte ATN-Schema bedient sich der momentan in der Patientenversorgung zur Verfügung stehenden Biomarker und beschreibt rein deskriptiv die vorhandenen Pathologien.
- A steht wenig überraschend für die ß-Amyloid-Pathologie, die entweder per nuklearmedizinischer Diagnostik oder als Amyloid-ß 42 bzw. Amyloid-ß 42 / Amyloid-ß 40-Verhältnis im Liquor festgestellt wird
- T beschreibt die Tau-Protein-Pathologie, ebenfalls entweder aus einer nuklearmedizinischen Untersuchung resultierend oder – im klinischen Alltag deutlich häufiger – aus der Liquordiagnostik über den Gesamt-Tau- und phospho-Tau-Wert.
- N meint klinische oder bildmorphologische (MRT, FDG-PET) Zeichen der Neurodegeneration, die anders als die ß-Amyloid- und Tau-Protein-Veränderungen aber nicht spezifisch für die Alzheimer-Krankheit sind. Entsprechend können folgende ATN-Beschreibungen resultieren:
| ATN-Profil | Biomarkerkategorie | |
|---|---|---|
| A-T-N- | Unauffällige Biomarker | |
| A+T-N- | Pathologische Alzheimer-Veränderungen | Pathophysiologisches Kontinuum der Alzheimer-Krankheit |
| A+T-N+ | ||
| A+T+N- | Alzheimer-Krankheit | |
| A+T+N+ | ||
| A-T+N- | Pathologische Nicht-Alzheimer-Veränderungen | |
| A-T-N+ | ||
| A-T+N+ | ||
Dieses Vorgehen ermöglicht relativ präzise Alzheimer-Krankheitsstadien auf biologischer und nicht nur auf klinischer Ebene zu beschreiben und ist so Grundlage für eine spezifische krankheitsmodifizierende Therapie, hilft aber andererseits auch andere neurodegenerative Erkrankungen mit einzuordnen.
Durch das Thema Blut-Biomarker kam die Frage auf, wie gut und weit der Zeithorizont der Vorhersage einer Entwicklung einer Alzheimer-Krankheit bei auffälligen Liquor- und PET-Biomarkern ist. Hier ist die Studienlage insgesamt recht heterogen. Bestenfalls kann man mit unauffälligen, aber auch mit auffälligen Liquorparametern knapp 20 Jahre in die Zukunft schauen, schlechtestenfalls eher 2. Die meisten Arbeiten geben einen Zeithorizont – abhängig vom Krankheitsstadium – zwischen gut 5 und 10 Jahren an.
Bluttest für alle?
Die Idee, die bislang recht aufwändige Alzheimer-Diagnostik durch einen Bluttest zu vereinfachen ist nicht neu. In den letzten Jahren haben sich zwei phospho-Tau-Derivate als vielversprechendste Option herausgestellt, die man – in sehr niedriger Konzentration – auch im Blut messen kann und deren Plasma-Spiegel mit der phospho-Tau-Konzentration im Liquor gut korreliert: phospho-Tau-181 und phospho-Tau-217. Von diesen beiden hat sich in der letzten Zeit das zweite offenbar durchgesetzt und es gibt erste Labore (Link), die eine phospho-Tau-217-Bestimmung im Blut auch in Deutschland anbieten. Nicht zuletzt durch die eingangs zitierte Studie von Petersen et al. wurde dies auch noch mal medial in die Breite kommuniziert. Der Vorhersagehorizont von phospho-Tau-217 scheint je nach Alter – ebenfalls Krankheitsstadium – bei jungen Menschen bis zu 20 Jahre, bei älteren Menschen eher um 11 Jahre zu liegen.
Aber – wo Licht ist, ist auch Schatten: So spezifisch wie es zuletzt oft anklang, ist phospho-Tau-217 wohl doch nicht. In einer Studie (Abu-Rumeileh et al.) aus Deutschland konnte gezeigt werden, dass der Biomarker auch bei Menschen mit einer Amyotrophen Lateralsklerose (ALS) erhöht ist und entgegen der bisherigen Annahmen eben nicht nur aus dem Gehirn sondern auch aus der Muskulatur stammt. Diese Beobachtung passt aber wiederum auch zur ATN-Klassifikation. Eine Tau-Protein-Erhöhung ist eben nicht spezifisch für eine Alzheimer-Krankheit, sondern tritt sowohl nach akuter Hirnschädigung, aber auch im Rahmen anderer neurodegenerativer Erkrankungen auf. Zur Diagnose einer Alzheimer-Krankheit gehört eben auch die Feststellung pathologischer ß-Amyloid-Ablagerungen.
Somit wird es – zumindest mit phospho-Tau-217 als Biomarker – so schnell nichts mit: Wir screenen alle Menschen ab einem gewissen Alter und schauen wer wohl eine Alzheimer-Krankheit entwickelt und behandeln diese Personen dann krankheitsmodifizierend mit einer Antikörper-Therapie.
Wo man weiterlesen kann
Abu-Rumeileh S, Scholle L, Mensch A, et al. Phosphorylated tau 181 and 217 are elevated in serum and muscle of patients with amyotrophic lateral sclerosis. Nat Commun. 2025;16(1):2019.
Jack CR, Bennett DA, Blennow K, et al. A/T/N: An unbiased descriptive classification scheme for Alzheimer disease biomarkers. Neurology. 2016;87(5):539-547.
Petersen KK, Milà-Alomà M, Li Y, et al. Predicting onset of symptomatic Alzheimerʼs disease with plasma p-tau217 clocks. Nat Med. Published online February 19, 2026.
Scheltens P, De Strooper B, Kivipelto M, et al. Alzheimer’s disease. The Lancet. 2021;397(10284):1577-1590.
Weitere Literatur
Boerwinkle AH, Wisch JK, Chen CD, et al. Temporal Correlation of CSF and Neuroimaging in the Amyloid-Tau-Neurodegeneration Model of Alzheimer Disease. Neurology. 2021;97(1).
Bungenberg J, Costa AS, Reetz K. Von symptombasierter Diagnostik hin zu einem biologischen Konzept. NeuroTransmitter. 2022;33(3):36-43.
Li Y, Yen D, Hendrix RD, et al. Timing of Biomarker Changes in Sporadic Alzheimer’s Disease in Estimated Years from Symptom Onset. Annals of Neurology. 2024;95(5):951-965.
Raket LL, Binette AP, Mattsson-Carlgren N, Janelidze S. Estimating the time course of biomarker changes in Alzheimer’s disease.
Rani N, Moghekar A, Callow DD, et al. Association Between Longitudinal Rate of Change in CSF Biomarkers and Subsequent Tau PET Burden in Early Braak Stages. Neurology. 2026;106(4):e214620.
Ward A, Caro JJ, Kelley H, Eggleston A, Molloy W. Describing Cognitive Decline of Patients at the Mild or Moderate Stages of Alzheimer’s Disease Using the Standardized MMSE. International Psychogeriatrics. 2002;14(3):249-258.

Hinterlasse einen Kommentar