Das Vorgeplänkel
Andexanet alfa (Ondexxya) wurde 2019 als Antidot zur Behandlung lebensbedrohlicher Blutungen unter den direkten oralen Antikoagulanzien Apixaban (Eliquis) und Rivaroxaban (Xarelto) (beides Faktor Xa-Antagonisten) zugelassen. Während es mit Idarucizumab (Praxbind) schon seit 2015 ein hochwirksames spezifisches Gegenmittel für Dabigatran (Pradaxa) gab, nach dessen Gabe man auch Notfalleingriffe und auch Thrombolysen durchführen kann, klaffte bei den Faktor Xa-Antagonisten eine Lücke, bei Edoxaban (Lixiana) klafft sie bis heute.
Andexanet alfa ist im Grunde ein gentechnisch hergestellter Gerinnungsfaktor Xa, an welchen die Medikamente binden sollen, so nicht mehr an das körpereigene Xa binden können und dadurch die gerinnungshemmende Wirkung aufgehoben wird.
Zugelassen wurde Andexanet alfa mit den Daten der ANNEXA-4-Studie (Milling et al). Diese Studie untersuchte vor allem die hämostaselogische Wirksamkeit von Andexanet alfa an Patienten mit intrakraniellen (69%) aber auch gastrointestinalen Blutungen (23%). Endpunkte waren die Veränderung der Faktor Xa-Aktivität nach Gabe des Medikamentes und die Verhinderung eines Hämatomwachstums innerhalb von 12 Stunden nach Anwendung. Klinische Daten, die einen Einfluss auf Behinderungsgrad und Mortalität nach Blutungsantagonisierung zeigten, wurden seinerzeit nicht veröffentlicht, was verschiedentlich kritisiert wurde, v.a. weil dies bei Idarucizumab anders ist. Auflage der Zulassung war aber das Nachliefern weiterer prospektiv gewonnener Daten zur Gabe von Andexanet alfa bei Hirnblutungen im Vergleich zu einer üblichen Vergleichstherapie. Diese Studie wurde nun veröffentlicht.
Das Paper
Referenz:
Connolly SJ, Sharma M, Cohen AT, et al. Andexanet for Factor Xa Inhibitor–Associated Acute Intracerebral Hemorrhage. N Engl J Med. 2024;390(19):1745-1755.
Worum geht es?
In die ANNEXa-I-Studie wurden insgesamt 530 Patienten mit Hirnblutungen unter Apixaban oder Rivaroxaban eingeschlossene, das mittlere Alter lag bei 78,9 Jahren, 54% der Patienten waren männlich, 46% weiblich. Die Hirnblutungen mussten ein Volumen von mindestens 0,5 ml und maximal 60 ml aufweisen, die letzte Faktor Xa-Hemmer-Einnahme durfte maximal 15 Stunden zurückliegen. Die Patienten erhielten entweder Andexanet alfa oder eine „übliche Vergleichstherapie“ (in vielen Fällen Gerinnungsfaktoren wie PPSB). Da die Applikationsarten zu unterschiedlich waren erfolgte die Gabe unverblindet, die Auswertung der Studienergebnisse war aber verblindet.
Als primäre Endpunkte wurden die hämostatische Effizienz nach 12 Stunden gemessen an einem Hämatomwachstum < 20 % („exzellente Hämostase“) oder < 35 % („gute Hämostase), ein NIHSS-Anstieg < 7 Punkte nach 12 Stunden und die fehlende Notwendigkeit weiterer Notfalltherapien (z.B. OP, zusätzliche PPSB-Gabe usw..) nach 3 bis 12 Stunden festgelegt.
Die gerinnungstechnische Veränderung der Faktor Xa-Aktivität mit Erreichen des Nadirs nach zwei Stunden war der sekundäre Endpunkt, Sicherheitsendpunkte waren die Rate an thrombotischen Ereignissen 30 Tage nach Gabe von Andexanet alfa und die Mortalität ebenfalls nach 30 Tagen, zudem erfolgte eine Post Hoc-Analyse hinsichtlich des Behiderungsgrades an Tag 30 gemessen auf der modified Ranking Scale (mRS) und eingeteilt in ein gutes (mRS ≦ 3) und ein schlechtes (mRS > 3) Ergebnis.
Was kam raus?
Die primären Endpunkte wurden größtenteils erreicht, die Studie daher vorzeitig abgebrochen. Andexanet führte in 76,7% der Fälle zu einer guten oder exzellenten Hämostase, in der Vergleichsgruppe wurde dies nur in 64,6% erreicht. Allerdings gab es keinen Unterschied beim NIHSS und auch nicht bei der Notwendigkeit einer Rescue-Therapie.
Statistisch signifikant waren aber vermehrte thrombotische Ereignisse (10,3% vs. 5,6%) unter Andexanet alfa, dabei auch (statistisch nicht signifikant) ischämische Schlaganfälle (6,5% vs. 1,5%) und Todesfälle (27,8% bei Andexanet alfa vs. 25,5% in der Vergleichsgruppe). Die Autoren wenden hierzu ein, dass die Studie für statistisch belastbare Aussagen zur Mortalität nicht genug Probanden eingeschlossen hat („nicht genug gepowert“). Das Fazit der Studienautoren lautet also:
In patients with ICH who were receiving FXa inhibitors, treatment with andexanet resulted in better control of hematoma expansion than usual care but was associated with thrombotic events.
und
However, in the current trial, multiplicity unadjusted results for death and a good outcome on the modified Rankin scale did not differ appreciably between groups; the trial was not designed to have sufficient power to detect differences in these outcomes.
Aber ist das so? Einordnung der Studienergebnisse
Es gibt ein paar (wenige) weitere Arbeiten, die sich mit dem Outcome nach Gabe verschiedener Antidots bei Antikoagulanzienblutungen beschäftig haben, z.B. eine Metaanalyse von Chaudhary et al. Hier wurden 32 – meist kleine und retrospektive – Studien mit insgesamt 1.832 Teilnehmern eingeschlossen. Man kann und muss diese Daten sicherlich mit Vorsicht betrachten, aber wenn man sie neben die ANNEXa-I-Studie stellt, fallen schon deutliche Parallelen auf:
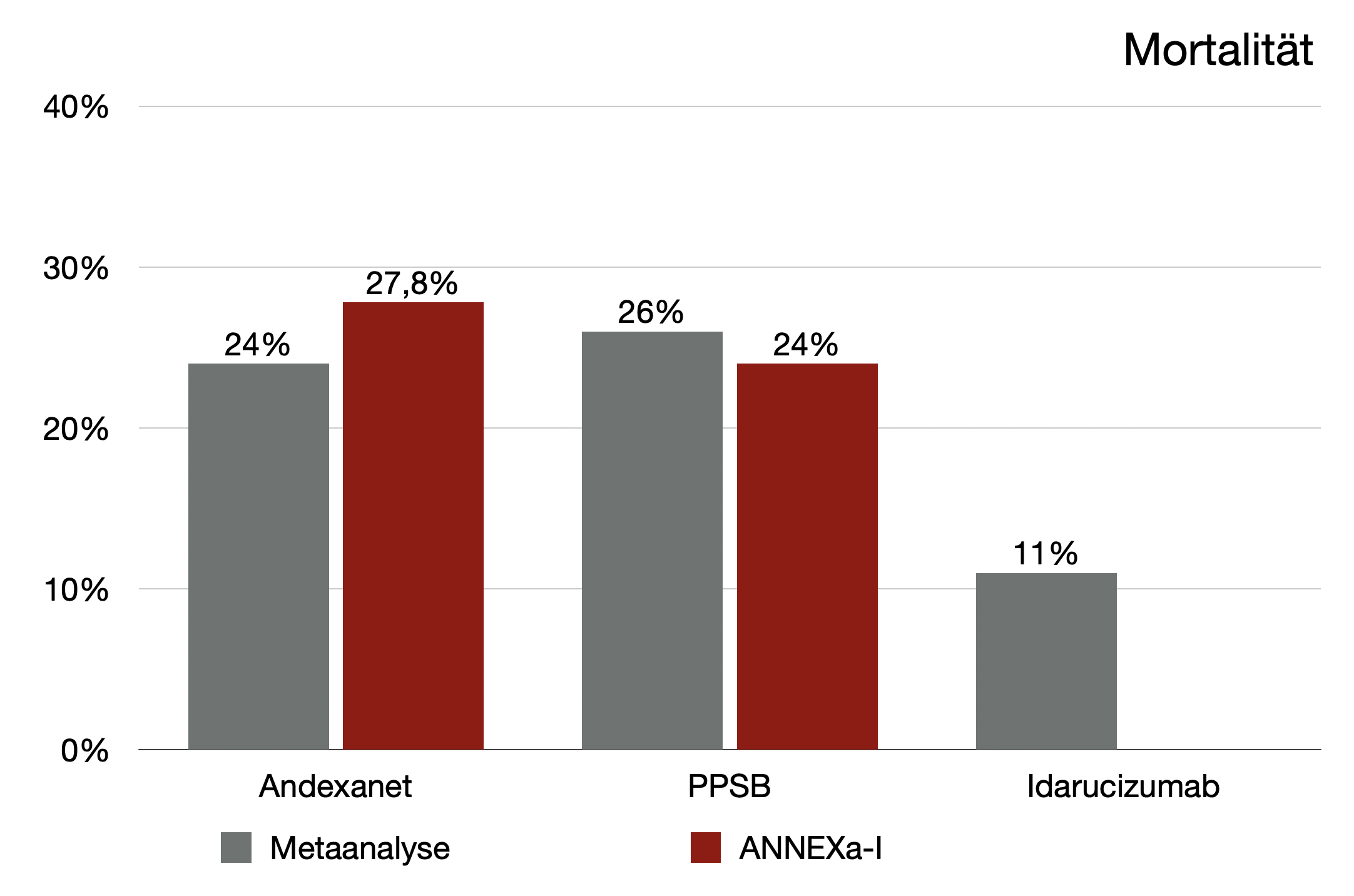
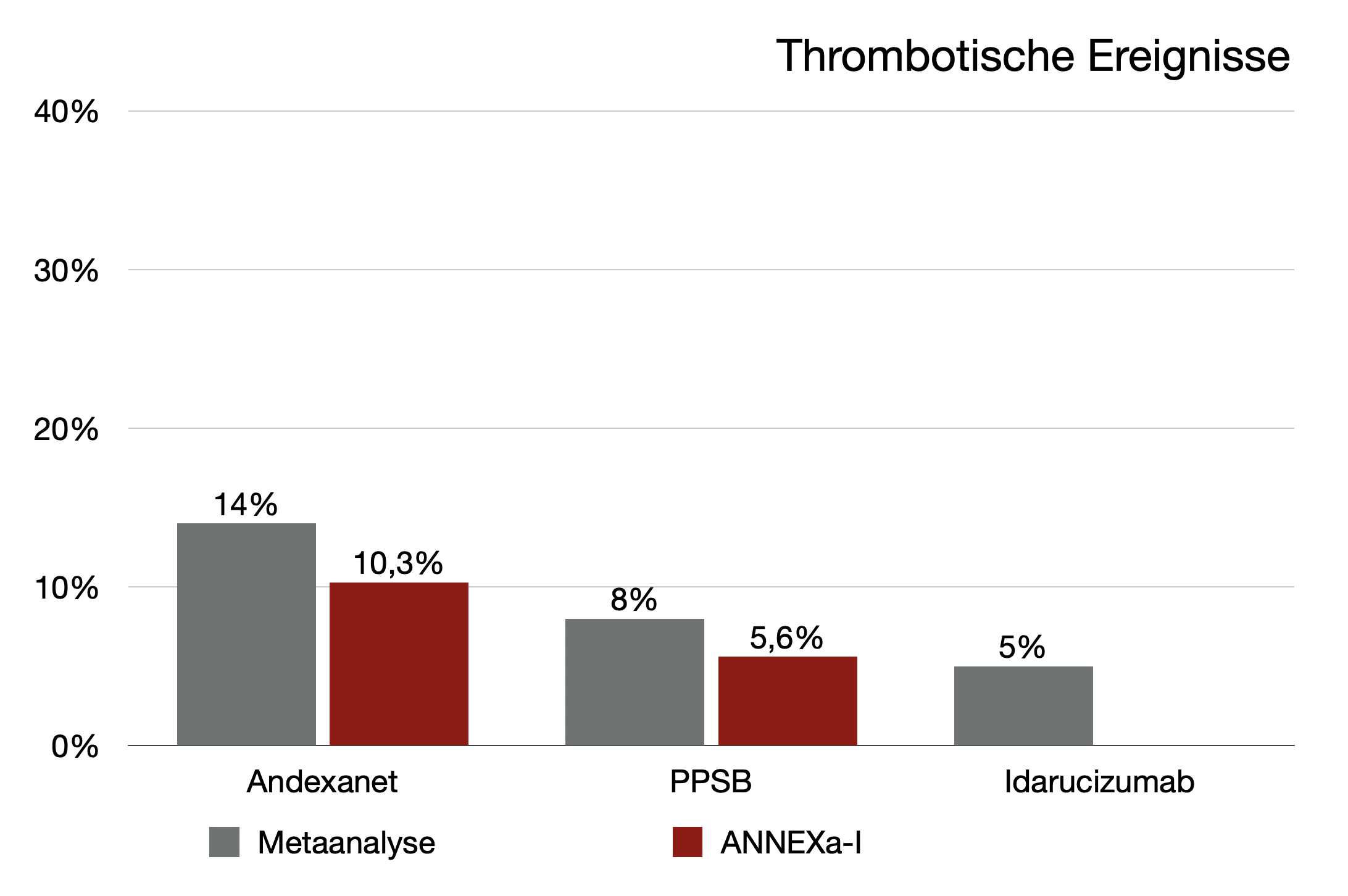
Nicht nur reproduzieren beide Arbeiten relativ gleiche Ergebnisse zur Mortalität und zur Rate thrombotischer Ereignisse, auch kann man feststellen, dass es zwischen PPSB und Andexanet kaum einen Unterschied zu geben scheint, wohl aber einen extremen zu Idarucizumab.
Die Elefanten im Raum
Es sind gleich zwei Elefanten, die da im Raum stehen.
Der eine ist die Frage, wie es passieren konnte, dass wenn man schon für die Zulassung die Ergänzung einer randomisierten Studie aufgetragen bekommt, diese keine klinische Endpunktstudie sein muss, sondern schlußendlich nur die Ergebnisse der schon bekannten ANNEXA-4-Studie reproduzieren soll. Ein. Erfolg des Pharmalobbyismus? Die Vermutung liegt zumindest nahe. Dass Andexanet alfa kein Gamechanger ist konnte man klinisch schon längst ahnen, nun hat man es schwarz auf weiß. Formal hat man nun aber die Zulassungsbedingungen erfüllt und die Wirksamkeit – im Rahmen der Auflagen – bewiesen. Es ist aber eine laborchemische Wirksamkeit und keine klinische.
Der zweite Elefant ist, ob denn PPSB eine Alternative zu Andexanet alfa wären. Das ist nicht so ganz leicht zu beantworten, weil es kaum Studien zur Gabe von PPSB bei NOAK-Blutungen gibt, vor allem nicht im Vergleich zu Placebo. Ein bisschen was findet man aber schon, z.B. die Arbeit von Gerner et al. In dieser retrospektiven Arbeit gab es bei einer Kohorte von 103 Blutungspatienten, die PPSB erhielten auch 43 Patienten, die nur nicht-medikamentös behandelt wurden. In dieser Arbeit schnitten die nicht mit PPSB behandelten Patienten nicht schlechter ab, als die mit PPSB behandelten, eine statistisch signifikante Wirksamkeit von PPSB konnte nicht gezeigt werden. Statistisch signifikant war nur die Senkung des systolischen Blutdrucks auf unter 160 mmHg.
Aus die Maus?
Eher nicht. Der Hype um Andexanet alfa hat in den Jahren seit der Zulassung merklich nachgelassen und auch der Preis ist gesunken, wenn er auch immer noch absurd hoch und deutlich höher als der von PPSB oder von Idarucizumab ist. Trotzdem wurde Andexanet alfa – auch schon vor der Veröffentlichung der Studienergebnisse – zuletzt immer zurückhaltender eingesetzt. Dies wird sich vermutlich weiter so fortsetzen und Andexanet da verwendet werden, wo das Verhinderung eines Hämatomwachstums wirklich eine entscheidende Rolle spielt, z.B. bei Blutungen in der hinteren Schädelgrube. Spannend werden die Reaktion und das Marketing von AstraZeneca, die Andexanet mittlerweile vertreiben, noch spannender die Positionierung von Fachgesellschaften und die Rolle die Andexanet in der im kommenden Jahr anstehenden Aktualisierung der DGN-Leitlinie Behandlung von spontanen intrazerebralen Blutungen (Link) spielen wird.
Wo man weiterlesen kann
Connolly SJ, Sharma M, Cohen AT, et al. Andexanet for Factor Xa Inhibitor–Associated Acute Intracerebral Hemorrhage. N Engl J Med. 2024;390(19):1745-1755.
Literatur
Chaudhary R, Singh A, Chaudhary R, et al. Evaluation of Direct Oral Anticoagulant Reversal Agents in Intracranial Hemorrhage: A Systematic Review and Meta-analysis. JAMA Netw Open. 2022;5(11):e2240145.
Gerner ST, Kuramatsu JB, Sembill JA, et al. Association of prothrombin complex concentrate administration and hematoma enlargement in non-vitamin K antagonist oral anticoagulant-related intracerebral hemorrhage. Ann Neurol. 2018;83:186–196.
Milling TJ, Middeldorp S, Xu L, et al. Final Study Report of Andexanet Alfa for Major Bleeding With Factor Xa Inhibitors. Circulation. 2023;147(13):1026-1038. doi:10.1161/CIRCULATIONAHA.121.057844
