Neuer Anlauf beim Zurück zum Neurologie-Content mit einem Brot-und-Butter-Neurologie-Thema: Der erste epileptische Anfall im Erwachsenenalter. Die dazugehörige DGN-Leitlinie ist abgelaufen und wird derzeit überarbeitet, parallel ist im vergangenen Jahr ist die SANAD II-Studie erschienen, mit der sich relevante Änderungen bei der First-Line-Medikation ergeben haben. Also muss ein Blogbeitrag her.
Epilepsie, unprovozierte und akut-symptomatische Anfälle
Epileptische Anfälle sind überhaupt nicht selten, 5-10% aller Menschen erleiden irgendwann im Leben einen epileptischen Anfall, viele davon einen Fieberkrampf als Kind oder einen nicht bemerkten epileptischen Anfall im Schlaf. Jedes Gehirn ist in der Lage einen epileptischen Anfall zu machen, nur die Schwelle, ab wann das passiert ist interindividuell unterschiedlich. Es gibt verschiedene Provokationsfaktoren wie metabolische Entgleisungen, Entzüge von GABA- und Gycin-erg wirkenden Substanzen wie Alkohol oder Benzodiazepinen, die zu epileptischen Anfällen führen können. Auch der berühmte Schlafmangel, über dessen Bedeutung durchaus kontrovers diskutiert wird, gehört dazu. In einem sehr sehr frühen brainpainblog-Beitrag hatte ich schon mal etwas zu diesen provozierten epileptischen Anfällen geschrieben, die früher auch Gelegenheitsanfälle oder Okkasionsanfälle genannt wurden und die mittlerweile als akut-symptomatische epileptische Anfälle bezeichnet werden.
Nomenklatur
Von einer Epilepsie spricht man, wenn zwei oder mehr nicht provozierte epileptische Anfälle im Abstand von mehr als 24 Stunden aufgetreten sind oder wenn es zu einem epileptischen Anfall „mit dem Wiederholungsrisiko von zwei Anfällen“ gekommen ist. Das klingt kompliziert, ist es aber nicht, dazu gleich mehr.
Mehrere epileptische Anfälle, die innerhalb von 24 Stunden auftreten heißen Serie epileptischer Anfälle, anhaltende epileptische Anfälle oder Serien bei denen der Patient zwischen den Anfällen das Bewusstsein nicht wiedererlangt Status epilepticus. Um den soll es heute aber nicht gehen, das ist ein eigenes Thema.
Epidemiologie
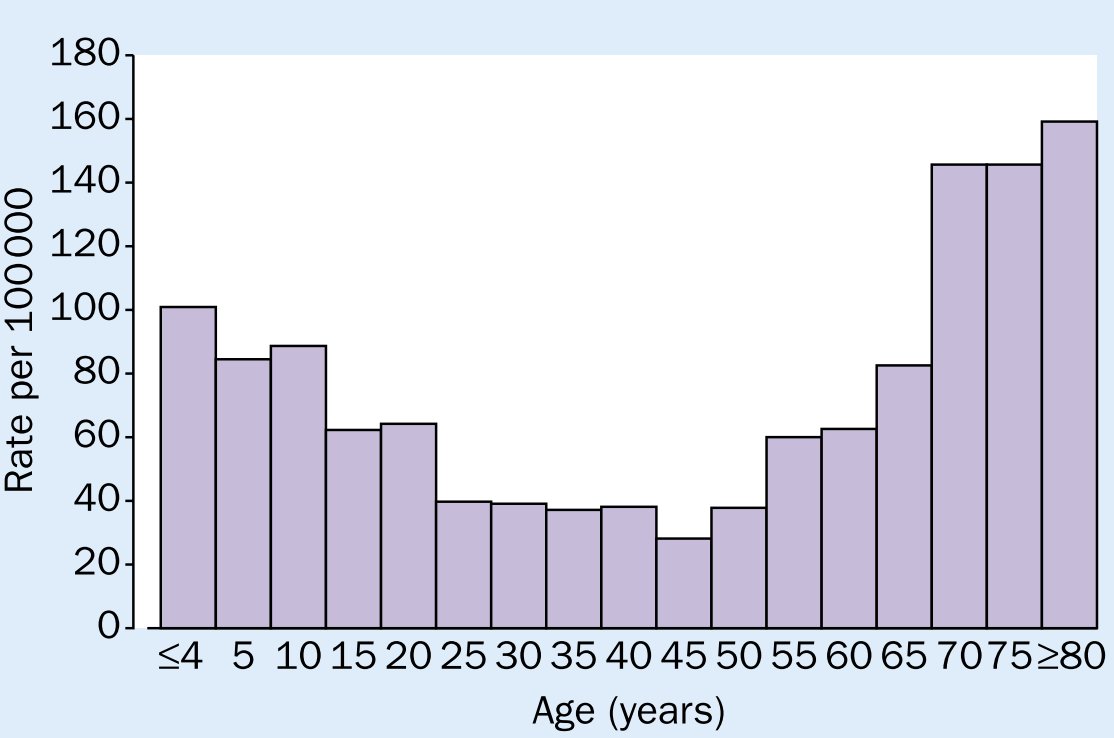
Die Epilepsie selber hat eine Inzidenz von 40-70/100.000 und eine Prävalenz von 500-900/100.000. Damit haben zwischen 0,5 und 0,9 Prozent der Bevölkerung eine Epilepsie. Diese Angaben sind aber nur bedingt hilfreich, da die Epilepsie-Inzidenz zwei sehr deutliche Altersgipfel hat, einmal im Kindes- und Jugendalter (bedingt durch die idiopathischen Epilepsien und den strukturell-läsionellen durch anlagebedingt und erworbene frühkindliche Hirnschäden) und im höheren Erwachsenenalter durch die dann auftretenden „erworbenen“ strukturellen Läsionen z.B. durch stattgehabte Schlaganfälle, Hirnblutungen oder Hirntumoren.
Risikostratifizierung
Die Epilepsie-Definition mit den „2 oder mehr nicht provozierten epileptischen Anfällen“ kommt immer so unhandlich daher, hat aber folgenden Hintergrund, der aus den Grafiken aus der Arbeit von Specht und Bien sehr eindrücklich hervorgeht.

Fangen wir mit Grafik d rechts unten an. Nach einem unprovozierten epileptischen Anfall liegt das Wiederholungsrisiko bei ca. 20%, steigt im Laufe von 5 Jahren noch auf 30%. Sobald ein zweiter Anfall auftritt landet man bei einem Wiederholungsrisiko von 60%, welches innerhalb der 5 Jahre Nachbeobachtungszeit auf ca. 70% steigt. Ein dritter Anfall ändert daran aber nichts mehr, hier bleibt das Risiko für einen vierten, fünften usw. Anfall dann gleich. Das ist die Rationale für die „2 oder mehr nicht provozierte epileptischen Anfälle“, die eine Epilepsie definieren.
Unter a sieht man das Wiederholungsrisiko nach mehreren unprovozierten epileptischen Anfällen und nach akut-symptomatischen Anfällen. Während es sich bei den unprovozierten epileptischen Anfällen um die 60% einpendelt, bleibt es bei den akut-symptomatischen Anfällen stabil bei 20%.
Grafik b verdeutlicht, dass der Schlafentzug viel weniger relevant ist, als man oft glaubt und das Wiederholungsrisiko nach einem epileptischen Anfall mit Schlafentzug eher beim nicht-provozierten als beim akut-symptomatischen Anfall liegt. Grafik c ist historisch bedeutsam und zeigt verschiedene Studien, die sich in den 1980er und 1990er Jahren an der Risikostratifizierung versucht haben.
Ob nach einem unprovozierten epileptischen Anfall ein weiterer Anfall auftritt und damit dann formal eine Epilepsie vorliegt ist vom Vorliegen verschiedener Risikofaktoren abhängig, die man sehr gut im Rahmen einer Epilepsie-Abklärung stratifizieren kann. Generell kann man sagen, dass kortikale Läsionen in der MRT, epilepsietypische EEG-Veränderungen und das Auftreten von epileptischen Anfällen aus dem Schlaf heraus weitere epileptische Anfälle wahrscheinlicher machen.
Auch hier hat die Arbeit von Specht und Bien eine hilfreiche Grafik.
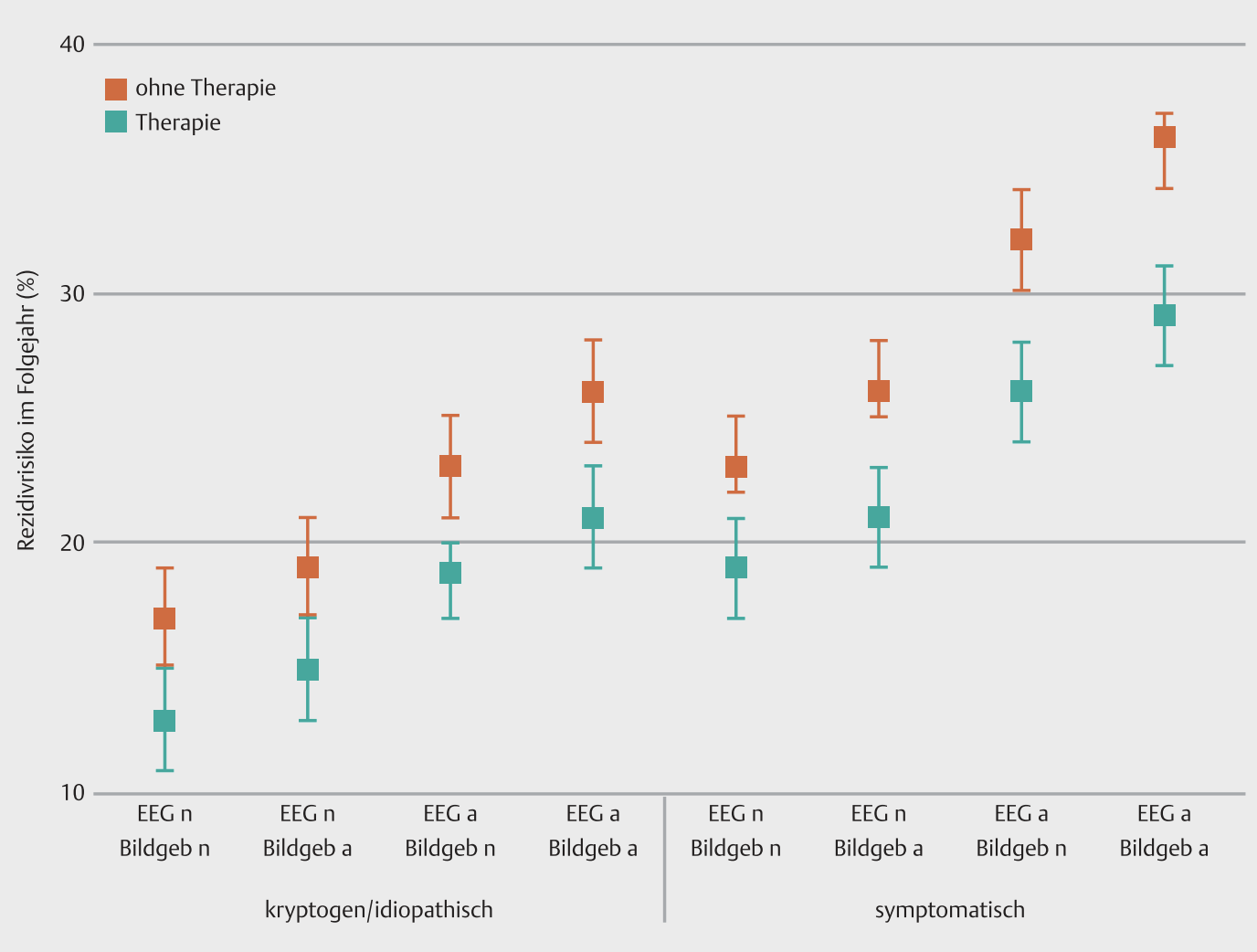
Links geht es um die (vermeintlich) idiopathischen epileptischen Anfälle, rechts um die strukturell-läsionellen. Man sieht, wie das Wiederholungsrisiko bei beiden Anfallsentitäten mit auffälligem EEG (a = auffällig, n = normal) oder MRT steigt. Das heißt, sind EEG und/oder MRT auffällig ist es relativ wahrscheinlich, dass eine Epilepsie vorliegt und weitere Anfälle zu erwarten sind, was sich mit der folgenden Grafik deckt, in der man sehen kann, dass eine antikonvulsive Therapie sich vor allem dann rentiert, wenn mehrere Anfälle aufgetreten sind oder die Epilepsie-Diagnostik auffällig geblieben ist.

Epilepsie-Diagnostik
Was gilt es nun zu tun, wenn sich ein Patient nach einem epileptischen Anfall ärztlich vorstellt? Eigentlich ist es ganz banal, man macht das, was man immer macht: Anamnese, körperliche Untersuchung, apparative und laborchemische Diagnostik. Bei all diesen Dingen gibt es ein paar Punkte, auf die es zu achten gilt.
Anamnese
Bei einem epileptischen mit Bewusstseinsverlust erwarten wir in der Regel eine ordentliche mnestische Lücke. Das heißt, eine sofortige Reorientierung spricht eher für eine stattgehabte Synkope oder einen psychogenen nicht epileptischen Anfall (PNEA). Typisch sind Eigenanamnesen, in denen die Patienten berichten, plötzlich oder nach einer Aura das Bewusstsein verloren zu haben und erst beim Eintreffen des Rettungsdienstes, im Rettungswagen oder im Krankenhaus sich erst wieder an die Geschehnisse erinnern zu können. Muskelkater wird nach generalisierten epileptischen Anfällen oft erst am Folgetag berichtet.
Viel hilfreicher ist aber oft die Fremdanamnese. Zum Einen ist bei Anfällen mit Bewusstseinsverlust die Frage nach den Augen des Betroffenen hilfreich, wie die Grafik aus der DGN-Leitlinie verdeutlicht:

Die Augenstellungen bei A1 und A2 (der berühmte Herdblick) sprechen für einen epileptischen Anfall, geschlossene Augen (B) eher für einen psychogenen nicht epileptischen Anfall und nach oben verdrehte, leicht geöffnete Augen (oft mit „flatternden“ Augenlidern) für Synkopen.
Auch das Hautkolorit des Patienten ist oft hilfreich: Gerade bei kardinalen Synkopen sind die Patienten oft aschfahl, bei vasovagalen kaltschweißig. Und schlussendlich kann man nach der Dauer des Anfalls fragen, wobei diese oft grandios überschätzt wird und vor allem dann verwertbar ist, wenn jemand auf eine Uhr geschaut hat. Ein typischer generalisierte epileptischer Anfall dauert 90 bis 120 Sekunden, bei Synkopen wird in der Regel innerhalb von 30 Sekunden das Bewusstsein wiedererlangt, Anfälle über 10 Minuten sind – wenn sie kein Status epilepticus sind, was manchmal echt schwierig zu differenzieren ist – hochverdächtig auf psychogene nicht epileptische Anfälle.
Klinische Untersuchung
Relativ typisch für einen generalisierten epileptischen Anfall ist ein lateraler Zungenbiss, während Zungenbissverletzungen an der Zungenspitze durchaus auch bei Synkopen oder psychogenen nicht-epileptischen Anfällen auftreten können. Des Weiteren lohnt es sich gerade bei jüngeren muskulösen Anfallspatienten per Klopfen eine Wirbelsäulenfraktur unwahrscheinlich zu machen, da diese bei generalisierten (tonisch-klonischen) Anfällen recht häufig auftreten.
Bildgebung
Standard-Bildgebung nach einem stattgehabten epileptischen Anfall, bzw. in der Anfallsabklärung ist heutzutage ein MRT, welches bei nicht zwingend mit Kontrastmittel erfolgen muss. Immer wenn es eine Tumoranamnese gibt und nun einen epileptischen Anfall sollten jedoch KM-Sequenzen angefertigt werden, da Mikrometastasen oder eine Meningeosis carcinomatosa durchaus epileptische Anfälle verursachen kann und in den Sequenzen ohne KM nicht zwingend auffällt.
Bei jüngeren Patienten wird nach anlagebedingten Anomalien gesucht, z.B. eine Temporalhorn-Sklerose oder im Marklager versprengten Kortexinseln (Heterotopien), bei älteren Patienten eher nach abgelaufenen Schlaganfällen, Hirnblutungen und ggfs. nach Tumoren.
EEG
Die Chance im interiktualen EEG – also der EEG-Ableitung nach, bzw. zwischen zwei Anfällen – Pathologien abzuleiten ist nicht besonders hoch. Man schätzt, dass man nur in 20 bis 40% der Fälle nach einem Anfall epilepsietypische Potentiale ableiten kann, die Sensitivität ggfs. vorhandene epilepsietypische Potentiale abzuleiten liegt dann nach drei EEG-Ableitung auch gerade mal bei 70%. Findet man sie, ist das (siehe Risikostratifizierung) ein relativ harter Indikator für das Auftreten weiterer epileptischer Anfälle. Nach derzeitigem Wissensstand sind diese dann bei 77% der Menschen mit einem pathologischen EEG nach einem stattgehabten epileptischen Anfall zu erwarten.

Allerdings haben auch zwischen 0,5 und 2% aller Menschen, die nicht an einer Epilepsie leiden zwischendurch epilepsietypische Muster im EEG und bestimmte Medikamente – v.a. Neuroleptika – führen zu derartigen Entladungsmustern im EEG ohne dass die Patienten an einer Epilepsie leiden (wobei Neuroleptika nahezu alle die „Anfallschwelle“ senken).
Labordiagnostik
Laborchemisch ist vor allem die CK interessant, welche bei generalisierten epileptischen, tonisch-klonischen Anfällen mit einer Sensitivität von bis zu 88% und einer Spezifität von 85 bis 100% zwischen bilateral tonisch-klonischen und psychogenen nicht-epileptischen Anfällen unterscheiden kann, wenn man sie mehr als 12 Stunden nach dem Anfall bestimmt. Bei Synkopen ist die CK auch hilfreich, da ist die Sensitivität mit maximal 75% aber schlechter.
Prolaktin, was noch durch viele Köpfe spukt lässt sich nur in Epilepsiezentren mit entsprechender Expertise sinnhaft bestimmen. Zum Einen benötigt man einen Basiswert, der aber interindividuell unterschiedlich ist und den man typischerweise nur dann bestimmt, wenn man Patienten hinsichtlich des Auftretens epileptischer Anfälle über einen gewissen Zeitraum beobachten will, wie es in Epilepsiezentren mit Video-EEG-Überwachung üblich ist. Eine Erhöhung auf mehr als das Dreifache des Basiswertes 15 bis 20 Minuten nach einem bilateral tonisch-klonischen Anfall hat dabei eine sehr hohe Sensitivität und Spezifität. Allerdings muss Prolaktin gekühlt ins Labor, umgehend bestimmt werden usw. und das klappt nur, wenn man gut geübte entsprechende Abläufe etabliert hat. Für die Wald und Wiesen-Neurologie ist das dementsprechend nichts, da ist die CK-Bestimmung nach 12 Stunden sinnvoller. Manchmal fällt – als Analogie zum Prolaktin – bei Patienten, die nach einem epileptischen Anfall aufgenommen werden und dort eine typische ZNA-Routine-Labordiagnostik abgenommen wird eine isolierte TSH-Erhöhung auf ohne dass eine Schilddrüsenfunktionsstörung vorliegt, die sich dann im Verlauf rasch normalisiert. Evidenzbasierten ist das aber nicht.
Wann braucht es eine Liquordiagnostik? Die (abgelaufene) Leitlinie hatte sich dazu gar nicht positioniert. Generell kann man sagen, immer wenn eine erregerbedingte oder autoimmun vermittelte Enzephalitis im Raum steht. Verkürzt gesagt also bei
- jungen Patienten mit psychiatrischer und/oder autonomer Dysregulation und epileptischen Anfällen und
- bei Patienten mit MRT-morphologischen Veränderungen, die an eine limbische Enzephalitis denken lassen unter dem Verdacht einer Autoimmunenzephalitis
- bei älteren Patienten mit Fieber, einem Anfall, v.a. wenn postiktual eine Aphasie auffällt mit der Frage vor allem nach einer Herpes-Enzephalitis.
Im Artikel von Malter findet sich passend hierzu folgende Aussage:
Es existieren jedoch keine hinreichenden Daten zur Sinnhaftigkeit einer Liquordiagnostik bei wachen, afebrilen Patienten nach erstem Anfall ohne weiteres fokales Defizit, weshalb diese nicht zwingend empfohlen wird.
Allerdings – wenn man die Indikation zur Liquorpunktion so streng auslegt – wird man durchaus vor allem „mildere“ Virusenzephalitiden und so zeigt die Erfahrung auch einige Autoimmunenzephalitiden verpassen. Momentan hilft vor allem etwas klinische Erfahrung bei der Einschätzung, es ist zu hoffen, dass die neue Leitlinie hier einen Algorithmus vorgibt. Wir halten es in der Regel so, dass wir wenn es eine klare strukturell-läsionelle Ursache gibt (wie einen stattgehabten Schlaganfall) oder wir im EEG bei jüngeren Patienten epilepsietypische Muster passend zu einer juvenilen idiopathischen Epilepsie finden keine Liquorpunktion durchführen, bei den ganz klaren Indikationen (siehe oben) diese in jedem Fall durchführen und bei den Fällen dazwischen sie zumindest niedrigschwellig anbieten.
Antikonvulsive Behandlung
Wann und warum behandeln?
Was sind jetzt Gründe für eine antikonvulsive Behandlung, bei der man ja in der Regel zweimal täglich sehr regelmäßig ein Medikament einnehmen muss? Man kann diese wie folgt zusammenfassen:
- Ein erhöhtes Rezidivrisiko
- nicht kausal zu behandelnde, bleibende Anfallsursachen (wie eine Schlaganfallnarbe, eine Hippocampussklerose u.ä.)
- eine gute Prognose für Anfallsfreiheit unter antikonvulsiver Medikation
- berufliche Risiken oder Wartefristen bei Epilepsie
- die Notwendigkeit Auto zu fahren
- Gefährdung durch Stürze durch die Anfälle, z.B. bei Indikation zur Einnahme einer antikonvulsiven Medikation und
- die persönliche Präferenz
Womit behandeln? Die blaue oder die rote Pille?
Ganz prinzipiell stehen eine ganze Menge Antikonvulsiva zur Verfügung, mit welchen man Epilepsien behandeln kann. Manche sind nur für die Behandlung primär generalisierter Epilepsien zugelassen, manche nur bei strukturell-läsionellen Anfallserkrankungen und gerade neuere Substanzen nur als And On-Therapie. Einen Überblick gibt diese Tabelle aus der 2017er DGN-Leitlinie, in der auch die in der Literatur oft verwendeten Abkürzungen für die einzelnen Antikonvulsiva aufgeführt sind:
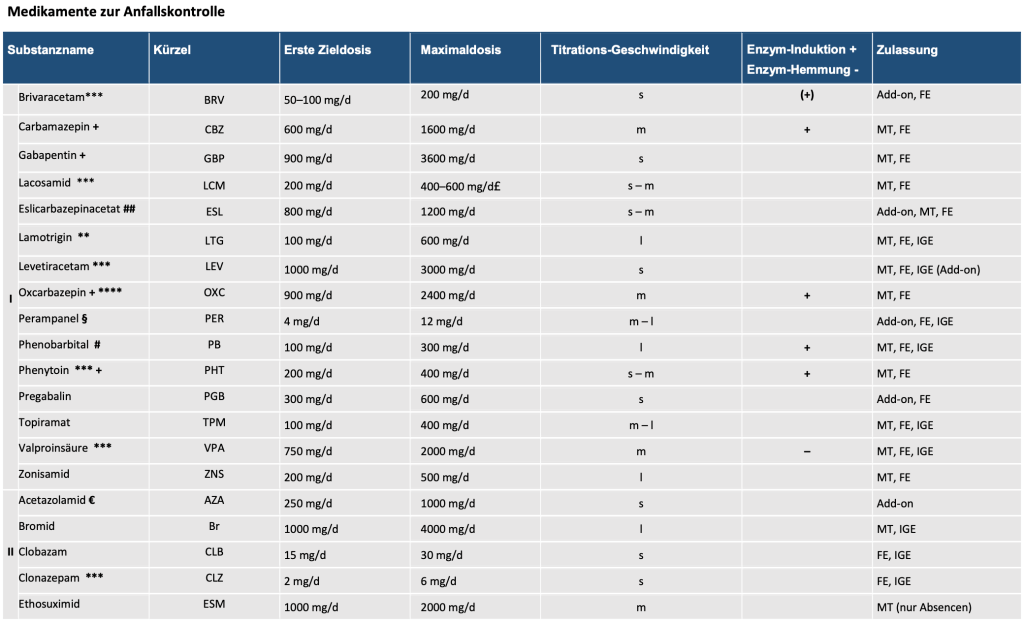

Am Ende ist es aber so wie mit den Opioiden. Jede/r braucht ein Medikament, mit dem sie oder er sich sicher und erfahren fühlt. Noch weiter schränkt sich die Auswahl durch die Leitlinienempfehlungen ein, die im Endeffekt wie folgt lauten:
Medikamente der ersten Wahl sind bei
- primär generalisierte Epilepsien: Valproat, Topiramat oder Lamotrigin
- fokale Epilepsien: Levetiracetam oder Lamotrigin
Dazu kommt noch die 2021 erschienene SANAD II-Studie, zu welcher es jeweils eine Publikation für generalisierte und eine für fokale Epilepsien gibt. In beiden Publikationen schnitt das in der Leitlinie noch als gleichwertig angesehene – und im klinischen Alltag oft auf Grund der schnellen Eindosierbarkeit und den fehlenden Medikamenteninteraktionen favorisierte – Levetiracetam schlechter ab als Valproat in der einen und Lamotrigin in der anderen Arbeit ab; und zwar sowohl in der Anfallskontrolle, als auch im Nebenwirkungsprofil. Valproat ist bei primär generalisierten Epilepsien schon signifikant besser wirksam als Lamotrigin, so dass es bei Männern und Frauen im nicht gebärfähigen Alter als erste Option erwogen werden sollte. Beachtet man aber den Rote Hand Brief zu Valproat (Link), so ist Lamotrigin für viele Patienten, bei denen Zeit für die notwendige Eindosierung ist, ein gutes Präparat.
Alles hat ein Ende? Die Sache mit dem Absetzen
Gute Empfehlungen zum Absetzen von Antikonvulsiva gibt es eigentlich nicht. Lange Zeit wurde auf eine Arbeit von 1991 verwiesen, nun ist 2021 eine (relativ kleine) Studie mit 133 Epilepsie-Patienten erschienen (Contento et al.), die das Absetzen von Antikonvulsiva untersucht hat. Patienten die mehr als zwei Jahre anfallsfrei waren und gleich auf das erste Antikonvulsivum angesprochen haben, haben die besten Chancen auch nach einem Absetzversuch anfallsfrei zu bleiben. Setzt man Antikonvulsiva ab, so sollte man das sehr langsam über mehrere Monate tun.
Literatur
Bast, T. et al. Erster epileptischer Anfall und Epilepsien im Erwachsenenalter. Aktuelle Neurol. 44, 603–636 (2017).
Brandt, C. Akut-symptomatische epileptische Anfälle: Inzidenz, Prognose und Aspekte der antiepileptischen Behandlung. Aktuelle Neurol. 39, 480–485 (2012).
Contento M, Bertaccini B, Biggi M, et al. Prediction of seizure recurrence risk following discontinuation of antiepileptic drugs. Epilepsia. 2021;62(9):2159-2170. doi:10.1111/epi.16993
Elger C. E., Berkenfeld R. (geteilte Erstautorenschaft) et al. S1-Leitlinie Erster epileptischer Anfall und Epilepsien im Erwachsenenalter. 2017. (abgelaufen): https://dgn.org/leitlinien/030-041-erster-epileptischer-anfall-und-epilepsien-im-erwachsenenalter-2017/
Malter, M. Erster epileptischer Anfall. DGNeurologie 2, 295–302 (2019).
Marson, A. et al: The SANAD II study of the effectiveness and cost-effectiveness of levetiracetam, zonisamide, or lamotrigine for newly diagnosed focal epilepsy: an open-label, non-inferiority, multicentre, phase 4, randomised controlled trial. The Lancet, 397(10282), 1363–1374. (2021) https://doi.org/10.1016/S0140-6736(21)00247-6
Marson, A., Burnside, G., Appleton, R., Smith, D., Leach, J. P., Sills, G., Tudur-Smith, C., Plumpton, C., Hughes, D. A., Williamson, P., Baker, G. A., Balabanova, S., Taylor, C., Brown, R., Hindley, D., Howell, S., Maguire, M., Mohanraj, R., Smith, P. E., … Jauhari, P. (2021). The SANAD II study of the effectiveness and cost-effectiveness of valproate versus levetiracetam for newly diagnosed generalised and unclassifiable epilepsy: an open-label, non-inferiority, multicentre, phase 4, randomised controlled trial. The Lancet, 397(10282), 1375–1386. https://doi.org/10.1016/S0140-6736(21)00246-4/
Specht, U. & Bien, C. Erster epileptischer Anfall im erwerbsfähigen Alter: Prognose-adaptiertes Management. Aktuelle Neurol. 45, 737–748 (2018).
Stephen, L. J. & Brodie, M. J. Epilepsy in elderly people. Lancet 355, 1441–1446 (2000)
Vollmar, C. & Noachtar, S. Bildgebende Diagnostik und EEG in der Differenzialdiagnose epileptischer Anfälle. Nervenarzt 88, 1119–1125 (2017).
Hinterlasse einen Kommentar